题目内容
某溶液中只可能含有下列离子中的几种(不考虑溶液中含的较少的H+和OH-):Na+、NH 、SO
、SO 、CO
、CO 、NO
、NO 。取200 mL该溶液,分为等体积的两份分别做下列实验。实验1:第一份加入足量的烧碱并加热,产生的气体在标准状况下为224 mL。实验2:第二份先加入足量的盐酸,无现象,再加入足量的BaCl2溶液,得固体2.33 g。下列说法正确的是
。取200 mL该溶液,分为等体积的两份分别做下列实验。实验1:第一份加入足量的烧碱并加热,产生的气体在标准状况下为224 mL。实验2:第二份先加入足量的盐酸,无现象,再加入足量的BaCl2溶液,得固体2.33 g。下列说法正确的是
A.该溶液中一定含有Na+,且c(Na+)≥0.1 mol·L-1
B.该溶液中可能含有Na+
C.该溶液中一定不含NO
D.该溶液中肯定含有NH 、SO
、SO 、CO
、CO 、NO
、NO
A
【解析】
试题分析:根据实验1:第一份加入足量的烧碱并加热,会产生气体224mL,证明含有NH4+,且物质的量为0.01mol;实验2:第二份先加入足量的盐酸,无现象,则一定不含有CO32-,再加足量的BaCl2溶液,得固体2.33g,证明一定含有SO42-,且物质的量为:2.33g÷233g/mol=0.01mol,根据溶液中的电荷守恒,则一定含有钠离子,且钠离子的浓度≥(0.01mol×2-0.01mol)÷0.1L=0.1mol?L?1。A、根据溶液中NH4+物质的量为0.01mol,SO42-物质的量为0.01mol,根据电荷守恒则c(Na+)≥0.1 mol/L,故A正确;B、该溶液中一定含有Na+,故B错误;C、该溶液中可能含有NO3-,故C错误;D、该溶液中肯定含有NH4+、S042-、Na+,故D错误。
考点:本题考查离子的检验及推断、化学计算。

练习册系列答案
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案
相关题目

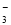 +2OH-===CaCO3↓+CO
+2OH-===CaCO3↓+CO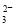 +2H2O
+2H2O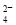 +3Cl-+5H2O
+3Cl-+5H2O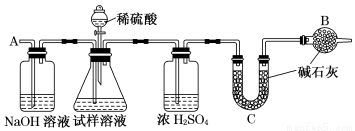
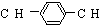 ,则M的结构式共有
,则M的结构式共有 
