题目内容
下列说法正确的是( )
| A、在氧化还原反应中金属单质只作还原剂 |
| B、有单质参加的化学反应一定是氧化还原反应 |
| C、金属阳离子被还原一定得到相应的金属单质 |
| D、金属氧化物一定是碱性氧化物 |
考点:氧化还原反应
专题:氧化还原反应专题
分析:A.金属单质化合价为最低价态;
B.同素异形体之间的转化为非氧化还原反应;
C.如为变价金属,则不一定得到单质;
D.金属氧化物可能为两性氧化物.
B.同素异形体之间的转化为非氧化还原反应;
C.如为变价金属,则不一定得到单质;
D.金属氧化物可能为两性氧化物.
解答:
解:A.金属单质化合价为最低价态,在反应中只能被氧化,表现为还原性,故A正确;
B.如氧气和臭氧之间的反应,都是单质,但为非氧化还原反应,故B错误;
C.如Fe3+→Fe2+,没有生成单质,故C错误;
D.金属氧化物可能为两性氧化物,如氧化铝,故D错误.
故选A.
B.如氧气和臭氧之间的反应,都是单质,但为非氧化还原反应,故B错误;
C.如Fe3+→Fe2+,没有生成单质,故C错误;
D.金属氧化物可能为两性氧化物,如氧化铝,故D错误.
故选A.
点评:本题考查氧化还原反应以及元素化合价知识,为高频考点,侧重于学生的分析能力和基础知识的综合理解和运用的考查,难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
若某共价化合物分子只含有C、H、N、O四种元素,且以n(C)、n(N)和n(O)分别表示C、N和O的原子数目,则H原子数目最多等于( )
| A、4n(C)+3n(N)+2n(O) |
| B、3n(C)+2n(N)+2 |
| C、2n(C)+n(N)+2 |
| D、2n(C)+n(N)+n(O)+2 |
下列反应的离子方程式书写正确的是( )
| A、稀H2SO4与铁粉反应:2Fe+6H+=2Fe3++3H2↑ |
| B、氢氧化钡溶液与稀硫酸反应:Ba2++SO42-=BaSO4↓ |
| C、氯化铜溶液与铁粉反应:Cu2++Fe=Fe2++Cu |
| D、碳酸钙与盐酸反应:CO32-+2H+=H2O+CO2↑ |
下列说法正确的是( )
| A、常温常压下,11.2L氮气所含的原子数为NA |
| B、常温常压下,1mol O3含有的核外电子数为4NA |
| C、18水所含的电子数目为10NA |
| D、同温同压下,相同体积的任何气体单质所含的原子数目相同 |
标准状况下,32g某气体的分子数与22gCO2的分子数相同,则该气体的摩尔质量为( )
| A、32 |
| B、32 g/mol |
| C、64g/mol |
| D、64 |
 右表为元素周期表前四周期的一部分,下列有关W、X、Y、Z四种元素的叙述中,正确的是( )
右表为元素周期表前四周期的一部分,下列有关W、X、Y、Z四种元素的叙述中,正确的是( )| A、与氢原子形成的化学键的键能:W比Y的大 |
| B、与氢原子形成的化学键的极性:X比Y的弱 |
| C、最低价气态氢化物的沸点:X的比W的高 |
| D、XZ3的晶体属于离子晶体 |
新能源的特点是资源丰富,无污染或很少污染,且可以再生.下列属于新能源的是( )
| A、太阳能 | B、石油 | C、天然气 | D、煤 |
下列电离方程式书写错误的是( )
| A、CaCl2=Ca2++2Cl- |
| B、NaHSO4=Na++H++SO42- |
| C、HNO3=H++NO3- |
| D、KOH=K++O2-+H+ |
| E、KOH=K++O2-+H+ |
下列物质既能发生消去反应,又能氧化成醛的是( )
| A、CH3CHOHCH3 |
B、 |
C、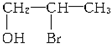 |
D、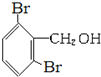 |