题目内容
2.下列叙述正确的是( )| A. | 过氧化钠与水反应生成氢氧化钠,则过氧化钠是碱性氧化物 | |
| B. | 钾、钠等碱金属着火时,立即用水或泡沫灭火器来灭火 | |
| C. | 用焰色反应可以检验钠的化合物跟钾的化合物 | |
| D. | 钠是一种还原性很强的金属,能把铜从硫酸铜溶液中置换出来 |
分析 A.碱性氧化物是能和酸反应只生成盐和水的氧化物;
B.钠、钾和水反应生成氢气,其燃烧产物都与和水、二氧化碳反应;
C.钠的焰色反应为黄色,钾的焰色反应为紫色,可以用焰色反应鉴别;
D.钠与硫酸铜溶液反应生成氢氧化铜沉淀、硫酸钠和氢气,不会生成铜单质.
解答 解:A.过氧化钠能与酸反应除了生成盐和水,还生成氧气,不符合碱性氧化物定义,故A错误;
B.钾和钠都能够与水反应生成可溶性气体氢气,二者的燃烧产物都能够与二氧化碳反应,所以不能用水、泡沫灭火器灭火,可以用砂子灭火,故B错误;
C.钾和钠元素的焰色反应呈现的火焰颜色不同,则可用焰色反应可以检验钠的化合物跟钾的化合物,故C正确;
D.钠与硫酸铜溶液反应时,钠先与水反应,然后生成的氢氧化钠与硫酸铜溶液反应生成氢氧化铜沉淀和硫酸钠,不会生成铜,故D错误;
故选C.
点评 本题考查了钠及其化合物性质,题目难度不大,涉及焰色反应、碱性氧化物判断、钠的化学性质等知识,明确常见元素及其化合物性质为解答关键,试题培养了学生的分析能力及灵活应用能力.

练习册系列答案
 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案
相关题目
7.几种短周期元素的原子半径及主要化合价如下表所示:
下列说法中正确的是( )
| 元素符号 | X | Y | Z | W |
| 原子半径/pm | 160 | 143 | 70 | 66 |
| 主要化合价 | +2 | +3 | +5,+3,-3 | -2 |
| A. | 一定条件下,Z的单质与W的常见单质直接生成ZW2 | |
| B. | Z最高价氧化物对应水化物与其氢化物能发生化合反应生成离子化合物 | |
| C. | Y的最高价氧化物对应水化物溶于氨水 | |
| D. | 相同条件下,X,Y的单质分别与盐酸反应时,后者反应剧烈些 |
7.下列图示实验操作,能达到目的是( )
| A. |  检验K+的存在 | B. |  | C. |  蒸馏 蒸馏 | D. |  检查气密性 |
12.下列离子方程式中,不正确的是( )
| A. | 向FeBr2溶液中通入少量的Cl2:2Fe2++Cl2═2Fe3++2Cl- | |
| B. | 向NH4Al(SO4)2溶液中滴入Ba(OH)2恰好使SO42-反应完全:2Ba2++4OH-+Al3++2SO42-═2BaSO4↓+AlO2-+2H2O | |
| C. | 向Ca(HCO3)2溶液中加入过量的NaOH溶液:Ca2++2HCO3-+2OH-═CaCO3↓+CO32-+2H2O | |
| D. | 向Fe(NO3)2溶液中加入稀盐酸:3Fe2++4H++NO3-═3Fe3++NO↑+2H2O |
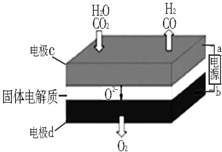 综合利用CO2、CO对构建低碳社会有重要意义.
综合利用CO2、CO对构建低碳社会有重要意义.