题目内容
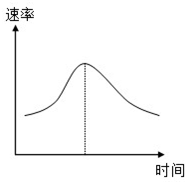 氯酸钾和亚硫酸氢钠发生氧化还原反应生成Cl(-1价)和S(+6价)的速率如图曲线所示,已知ClO3-的氧化性随c(H+)的增大而增强,有关方程式为:ClO3-+3HSO3-?Cl-+3H++3SO42-
氯酸钾和亚硫酸氢钠发生氧化还原反应生成Cl(-1价)和S(+6价)的速率如图曲线所示,已知ClO3-的氧化性随c(H+)的增大而增强,有关方程式为:ClO3-+3HSO3-?Cl-+3H++3SO42-(1)反应开始时反应速率加快的原因是
(2)反应后期反应速率下降的原因是
考点:化学反应速率的影响因素
专题:化学反应速率专题
分析:由图可知,反应速率先增大,后减小,开始与氢离子浓度有关,后来与反应物浓度有关,以此来解答.
解答:
解:(1)反应开始时反应速率加快,由ClO3-+3HSO3-?Cl-+3H++3SO42-可知,反应开始时随着反应的进行,c(H+)不断增大,反应的速率加快由题目信息可知反应的速率随c(H+)的增大而加快,故答案为:开始时随着反应的进行,c(H+)不断增大;
(2)反应后期反应速率下降,是因随着反应的进行,反应物的浓度减少,反应速率减小,故答案为:反应物浓度减小.
(2)反应后期反应速率下降,是因随着反应的进行,反应物的浓度减少,反应速率减小,故答案为:反应物浓度减小.
点评:本题考查化学反应速率的影响因素,为高频考点,把握习题中的信息及浓度对反应速率的影响为解答的关键,侧重分析能力及知识应用能力的考查,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列结论正确的是( )
| A、酸碱中和反应能生成盐和水,所以生成盐和水的反应一定是中和反应 |
| B、饱和溶液降低温度一定会析出晶体 |
| C、组成元素相同的物质化学性质不一定相同 |
| D、质子数相同的两种粒子其核外电子数一定相等 |
下列关于平衡常数的说法中,正确的是( )
| A、在平衡常数表达式中,反应物浓度用初始浓度,生成物浓度用平衡浓度 |
| B、在任何条件下,化学平衡常数是一个恒定值 |
| C、平衡常数的大小只与浓度有关,而与温度、压强、催化剂等无关 |
| D、从平衡常数的大小可以推断一个反应进行的程度 |
下列操作中不正确的是( )
| A、过滤时,玻璃棒与三层滤纸的一边接触 |
| B、过滤时,漏斗下方紧贴烧杯内壁 |
| C、加热试管内物质时,试管底部与酒精灯外焰接触 |
| D、向试管中滴加液体时,胶头滴管紧贴试管内壁 |
 化学对人类社会进步和发展的贡献之一是发现和研制了各种材料,例如,金属就是我们生活中不可或缺的重要材料,根据你学过的有关金属的知识,回答下列问题:
化学对人类社会进步和发展的贡献之一是发现和研制了各种材料,例如,金属就是我们生活中不可或缺的重要材料,根据你学过的有关金属的知识,回答下列问题:
