题目内容
四种短周期元素的微粒信息如下表:
已知Q、R、X在同一周期,R2在常温常压下为气态.完成下列填空:
(1)Q位于周期表第 周期 族.化合物Q2Z的电子式为 (元素符号表示)
(2)Q、R、X的原子半径由大到小的顺序为 .Q、R、X、Z中金属性最强的是 (元素符号表示)
(3)Q与X两者的最高价氧化物对应的水化物之间发生反应的离子方程式为 .
| 元素代号 | Q | R | X | Z |
| 微粒信息 | 离子 | 单质分子 R2 | 离子: X3+ | 一种原子 816Z |
(1)Q位于周期表第
(2)Q、R、X的原子半径由大到小的顺序为
(3)Q与X两者的最高价氧化物对应的水化物之间发生反应的离子方程式为
考点:原子结构与元素的性质
专题:元素周期律与元素周期表专题
分析:由四种短周期元素的微粒信息可知,Q的质子数为11,为Na;Z的质子数为8,则Z为O;Q、R、X在同一周期,且X为+3价,则X为Al;R2常温常压下为气体,R为Cl,然后结合元素的性质及化学用语来解答.
解答:
解:由四种短周期元素的微粒信息可知,Q的质子数为11,为Na;Z的质子数为8,则Z为O;Q、R、X在同一周期,且X为+3价,则X为Al;R2常温常压下为气体,R为Cl,
(1)Q位于第三周期第ⅠA族,化合物Q2Z的电子式为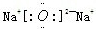 ,故答案为:三;ⅠA;
,故答案为:三;ⅠA;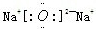 ;
;
(2)Q、R、X位于同周期,原子序数大的半径小,则原子半径由大到小的顺序为Na>Al>Cl,四种元素中只有Na、Al为金属,Na的金属性强,
故答案为:Na>Al>Cl;Na;
(3)Q与X两者的最高价氧化物对应的水化物之间发生反应的离子方程式为OH-+Al(OH)3=AlO2-+2H2O,故答案为:OH-+Al(OH)3=AlO2-+2H2O.
(1)Q位于第三周期第ⅠA族,化合物Q2Z的电子式为
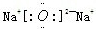 ,故答案为:三;ⅠA;
,故答案为:三;ⅠA;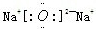 ;
;(2)Q、R、X位于同周期,原子序数大的半径小,则原子半径由大到小的顺序为Na>Al>Cl,四种元素中只有Na、Al为金属,Na的金属性强,
故答案为:Na>Al>Cl;Na;
(3)Q与X两者的最高价氧化物对应的水化物之间发生反应的离子方程式为OH-+Al(OH)3=AlO2-+2H2O,故答案为:OH-+Al(OH)3=AlO2-+2H2O.
点评:本题考查元素周期表的结构与应用,侧重位置、结构、性质的考查,把握元素的推断为解答的关键,注意元素周期律的应用,题目难度不大.

练习册系列答案
相关题目
有一种气体的质量是14.2g,物质的量是0.2mol,该气体的摩尔质量是( )
| A、28.4 |
| B、28.4g?mol-1 |
| C、71 |
| D、71g?mol-1 |
已知:HNCO(异氰酸,其结构是H-N=C=O)能和NO2反应生成N2、CO2和H2O.下列有关上述反应的叙述不正确的是( )
| A、HNCO中的氮元素被氧化 |
| B、NO2中的氮元素被还原 |
| C、每生成1mol H2O转移6mol电子 |
| D、CO2是氧化产物 |
我国自主研制可治疗H7N9禽流感新药帕拉米韦,结构如图.下列有关说法正确的是( )


| A、该有机物的分子式是C15H27O4N4 |
| B、该分子中含有氨基、羧基、羟基、醛基等官能团 |
| C、该分子不仅具有两性,还能发生水解反应和酯化反应 |
| D、该分子中含有6个手性碳原子 |
下列物质中,不能使品红溶液褪色的是( )
| A、Cl2 |
| B、SO3 |
| C、SO2 |
| D、活性炭 |

 2012年10月浙江省甲醇汽油试点评估完成,为浙江省甲醇汽油的进一步推广应用做好准备,与93号汽油相比,甲醇汽油每升约便宜0.5元-0.6元.已知常温常压下,1mol甲醇(CH3OH)(熔点-97.8℃、沸点64.5℃)在空气中完全燃烧生成液态水时,放出QkJ的热量.请回答下列相关问题:
2012年10月浙江省甲醇汽油试点评估完成,为浙江省甲醇汽油的进一步推广应用做好准备,与93号汽油相比,甲醇汽油每升约便宜0.5元-0.6元.已知常温常压下,1mol甲醇(CH3OH)(熔点-97.8℃、沸点64.5℃)在空气中完全燃烧生成液态水时,放出QkJ的热量.请回答下列相关问题: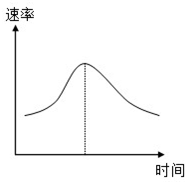 氯酸钾和亚硫酸氢钠发生氧化还原反应生成Cl(-1价)和S(+6价)的速率如图曲线所示,已知ClO3-的氧化性随c(H+)的增大而增强,有关方程式为:ClO3-+3HSO3-?Cl-+3H++3SO42-
氯酸钾和亚硫酸氢钠发生氧化还原反应生成Cl(-1价)和S(+6价)的速率如图曲线所示,已知ClO3-的氧化性随c(H+)的增大而增强,有关方程式为:ClO3-+3HSO3-?Cl-+3H++3SO42-