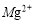题目内容
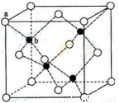
X、Y、Z、W是短周期元素,原子序数依次递增。X与Z位于同一主族,Y元素的单质既能与盐酸反应也能与NaOH溶液反应,Z原子的最外层电子数是次外层电子数的一半,Y、Z、W原子的最外层电子数之和为14。下列说法正确的是
A.气态氢化物的稳定性:X<Z <W
B.Y的阳离子半径比W的阴离子半径小
C.X、Z、W氧化物对应水化物酸性的强弱顺序为X<Z< W
D.室温下,含Y元素的盐形成的水溶液其pH<7
B
【解析】
试题分析:根据题意可推知这几种元素分别是X是C;Y是Al;Z是Si;W是Cl。A.元素的非金属性越强,其相应的氢化物的稳定性就越强。元素的非金属性Cl>C>Si,所以气态氢化物的稳定性:Z <X< W,错误;B.对于离子核外电子层结构不同的离子来说,离子核外电子层数越多,离子半径就越大,所以Y的阳离子半径比W的阴离子半径小,正确;C.元素的非金属性越强,其最高价氧化物对应的水化物的酸性就越强,元素的非金属性Cl>C>Si,所以X、Z、W氧化物对应水化物酸性的强弱顺序为Z<X<W,错误; D.室温下,含Y元素的盐如AlCl3是强酸弱碱盐,弱碱金属阳离子水解使形成的水溶液显酸性,其pH<7;而NaAlO2则是强碱与弱酸形成的盐,弱酸根离子AlO2-水解消耗水电离产生的H+,是溶液显碱性,pH>7,错误。
考点:考查元素的推断、元素形成的化合物的性质比较、盐的水解等知识。

(15分)高铁酸钾(K2FeO4)是一种高效多功能水处理剂,具有极强的氧化性。
(1)已知:4FeO42-+10H2O 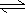 4Fe(OH) 3+8OH-+3O2↑。K2FeO4在处理水的过程中所起的作用有 。
4Fe(OH) 3+8OH-+3O2↑。K2FeO4在处理水的过程中所起的作用有 。
同浓度的高铁酸钾在pH为4.74、7.00、11.50的水溶液中最稳定的是pH= 的溶液。
(2)高铁酸钾有以下几种常见制备方法:
干法 | Fe2O3、KNO3、KOH混合加热共熔生成紫红色高铁酸盐和KNO2等产物 |
湿法 | 强碱性介质中,Fe(NO3)3与NaClO反应生成紫红色高铁酸盐溶液 |
电解法 | 制备中间产物Na2FeO4,再与KOH溶液反应 |
①干法制备K2FeO4的反应中,氧化剂与还原剂的物质的量之比为____ 。
②湿法制备中,若Fe(NO3)3加入过量,在碱性介质中K2FeO4与Fe3+发生氧化还原反应生成K3FeO4,此反应的离子方程式:____ ________________。
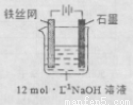
③制备中间产物Na2FeO4,可采用的装置如图所示,则阳极的电极反应
式为 。
(3)比亚迪双模电动汽车使用高铁电池供电,其总反应为:
3Zn+2K2FeO4+8H2O 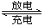 3Zn(OH)2+2Fe(OH)3+4KOH
3Zn(OH)2+2Fe(OH)3+4KOH
放电时负极材料为____ ,正极反应为:____ 。
(4) 25℃时,CaFeO4的Ksp=4.54×l0-9,若要使1000 L含有2.0×l0-4 mol·L-l K2FeO4的废水中的c(FeO42-)有沉淀产生,理论上至少加入Ca(OH)2的物质的量为____ mol。
 中的不同阳离子和阴离子各一种组成。已知:①将甲溶液分别与其他三种物质的溶液混合,均有白色沉淀生成;②0.1mol/L乙溶液中c(H+)>0.1mol/L;③向丙溶液中滴入
中的不同阳离子和阴离子各一种组成。已知:①将甲溶液分别与其他三种物质的溶液混合,均有白色沉淀生成;②0.1mol/L乙溶液中c(H+)>0.1mol/L;③向丙溶液中滴入 溶液有不溶于稀
溶液有不溶于稀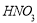 的白色沉淀生成,下列结论不正确的是
的白色沉淀生成,下列结论不正确的是  B.乙溶液含有
B.乙溶液含有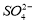 C.丙溶液含有
C.丙溶液含有 D.丁溶液含有
D.丁溶液含有