��Ŀ����
��15�֣�������أ�K2FeO4����һ�ָ�Ч���ˮ�����������м�ǿ�������ԡ�
��1����֪��4FeO42-+10H2O 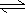 4Fe(OH) 3+8OH-+3O2����K2FeO4�ڴ���ˮ�Ĺ���������������� ��
4Fe(OH) 3+8OH-+3O2����K2FeO4�ڴ���ˮ�Ĺ���������������� ��
ͬŨ�ȵĸ��������pHΪ4.74��7.00��11.50��ˮ��Һ�����ȶ�����pH= ����Һ��
��2��������������¼��ֳ����Ʊ�������
�ɷ� | Fe2O3��KNO3��KOH��ϼ��ȹ��������Ϻ�ɫ�������κ�KNO2�Ȳ��� |
ʪ�� | ǿ���Խ����У�Fe��NO3��3��NaClO��Ӧ�����Ϻ�ɫ����������Һ |
��ⷨ | �Ʊ��м����Na2FeO4������KOH��Һ��Ӧ |
�ٸɷ��Ʊ�K2FeO4�ķ�Ӧ�У��������뻹ԭ�������ʵ���֮��Ϊ____ ��
��ʪ���Ʊ��У���Fe��NO3��3����������ڼ��Խ�����K2FeO4��Fe3+����������ԭ��Ӧ����K3FeO4���˷�Ӧ�����ӷ���ʽ��____ ________________��
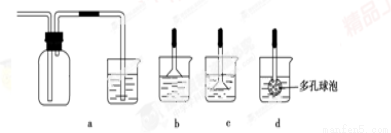
���Ʊ��м����Na2FeO4���ɲ��õ�װ����ͼ��ʾ���������ĵ缫��Ӧ
ʽΪ ��
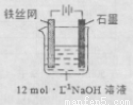
��3�����ǵ�˫ģ�綯����ʹ�ø�����ع��磬���ܷ�ӦΪ��
3Zn+2K2FeO4+8H2O 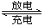 3Zn��OH��2+2Fe��OH��3+4KOH
3Zn��OH��2+2Fe��OH��3+4KOH
�ŵ�ʱ��������Ϊ____ ��������ӦΪ��____ ��
��4�� 25��ʱ��CaFeO4��Ksp=4.54��l0-9����Ҫʹ1000 L����2.0��l0��4 mol��L-l K2FeO4�ķ�ˮ�е�c��FeO42�����г������������������ټ���Ca��OH��2�����ʵ���Ϊ____ mol��
(1)K2FeO4����ǿ�����ԣ��ܹ�����ɱ����ͬʱFeO42�� ����ԭ��Fe3+��Fe3+ˮ���γ�Fe(OH)3���壬�ܹ�����ˮ���������ʣ�2�֣� 11.50��2�֣�
��2����3:1��2�֣�;�� 2FeO42����Fe3+��8OH����3FeO43����4H2O��2�֣�
��Fe+8OH����6e��=FeO42��+4H2O��2�֣�
��3��Zn��1�֣� FeO42��+4H2O+3e��== Fe(OH)3+5OH����2�֣�;��4��2.27��10-2��2�֣���
��������
�����������1����K2FeO4��Fe�Ļ��ϼ�Ϊ+6�ۣ�����ǿ�����ԣ��ܹ���ˮ����ɱ��������ͬʱFeO42�� ����ԭ��Fe3+��Fe3+ˮ���γ�Fe(OH)3���壬�������������ǿ���ܹ�����ˮ���������ʣ��Ӷ������������ã����ݷ���ʽ4FeO42-+10H2O 4Fe(OH) 3+8OH-+3O2����֪����������OH-��Ũ�ȣ�����ʹƽ�������ƶ����Ӷ����Լ�СFeO42-�ķ�Ӧ������Ӧ��ѡ����Һ����ǿ��pH=11.50����Һ����2���ٸɷ��Ʊ�K2FeO4�ķ�Ӧ��Fe2O3+2KNO3+4KOH
4Fe(OH) 3+8OH-+3O2����֪����������OH-��Ũ�ȣ�����ʹƽ�������ƶ����Ӷ����Լ�СFeO42-�ķ�Ӧ������Ӧ��ѡ����Һ����ǿ��pH=11.50����Һ����2���ٸɷ��Ʊ�K2FeO4�ķ�Ӧ��Fe2O3+2KNO3+4KOH K2FeO4��3KNO2+ 2H2O���ڸ÷�Ӧ��������KNO3�뻹ԭ��Fe2O3�����ʵ���֮��Ϊ3:1����ʪ���Ʊ��У���Fe(NO3) 3����������ڼ��Խ�����K2FeO4��Fe3+����������ԭ��Ӧ����K3FeO4���˷�Ӧ�����ӷ���ʽ��2FeO42����Fe3+��8OH����3FeO43����4H2O; ���Ʊ��м����Na2FeO4�������õ��ķ�����������Fe�ĵ缫��ӦʽΪFe+8OH����6e��=FeO42��+4H2O����3�����ǵ�˫ģ�綯����ʹ�ø�����ع��磬���ܷ�ӦΪ��3Zn+2K2FeO4+8H2O
K2FeO4��3KNO2+ 2H2O���ڸ÷�Ӧ��������KNO3�뻹ԭ��Fe2O3�����ʵ���֮��Ϊ3:1����ʪ���Ʊ��У���Fe(NO3) 3����������ڼ��Խ�����K2FeO4��Fe3+����������ԭ��Ӧ����K3FeO4���˷�Ӧ�����ӷ���ʽ��2FeO42����Fe3+��8OH����3FeO43����4H2O; ���Ʊ��м����Na2FeO4�������õ��ķ�����������Fe�ĵ缫��ӦʽΪFe+8OH����6e��=FeO42��+4H2O����3�����ǵ�˫ģ�綯����ʹ�ø�����ع��磬���ܷ�ӦΪ��3Zn+2K2FeO4+8H2O  3Zn��OH��2+2Fe��OH��3+4KOH�����ڷŵ�ʱ��������Ϊʧȥ����Ԫ�صĻ��ϼ����ߵ�����Zn���������ϵķ�ӦΪ��FeO42��+4H2O+3e��== Fe(OH)3+5OH����Ksp=c(Ca2+)��c(FeO42��)��4.54��l0-9��c(FeO42��)= 2.0��l0��4 mol/L,����c(Ca2+)��4.54��l0-9��c(FeO42��)= 4.54��l0-9��2.0��l0��4=2.27��10-5mol/L,���n(Ca��OH��2) ��2.27��10-5mol/L��1000L=2.27��10-2mol��
3Zn��OH��2+2Fe��OH��3+4KOH�����ڷŵ�ʱ��������Ϊʧȥ����Ԫ�صĻ��ϼ����ߵ�����Zn���������ϵķ�ӦΪ��FeO42��+4H2O+3e��== Fe(OH)3+5OH����Ksp=c(Ca2+)��c(FeO42��)��4.54��l0-9��c(FeO42��)= 2.0��l0��4 mol/L,����c(Ca2+)��4.54��l0-9��c(FeO42��)= 4.54��l0-9��2.0��l0��4=2.27��10-5mol/L,���n(Ca��OH��2) ��2.27��10-5mol/L��1000L=2.27��10-2mol��
���㣺�������ʵ���ȡԭ���ķ���ʽ��ʾ��������ԭ��Ӧ���йؼ��㡢���ʵ����ü������ܽ�ƽ���֪ʶ��

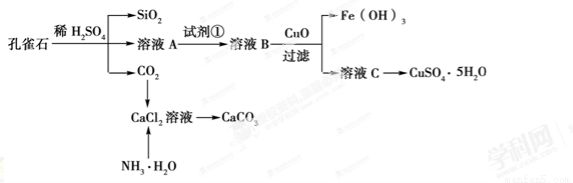

 2H2SO4
2H2SO4 +2H2O
+2H2O H2CO3+2OH?
H2CO3+2OH? +H2O
+H2O