题目内容
3.有关原电池的说法正确的是( )| A. | “Cu-Zn-硫酸”原电池中,电子从Zn经过导线到达Cu,再经过溶液回到Zn形成闭合回路 | |
| B. | “Al-Mg-NaOH”原电池中,活泼型强的Mg失去电子,被氧化,做负极 | |
| C. | 理论上所有自发进行的氧化还原反应均可设计成原电池 | |
| D. | 已知铅蓄电池总反应为:Pb+PbO2+2H2SO4=2PbSO4+2H2O,可推负极是反应是 Pb-2e-=Pb2+ |
分析 A.电子不能通过溶液;
B.金属镁和氢氧化钠溶液不能发生氧化还原反应,铝能与氢氧化钠溶液发生氧化还原反应,失电子的做负极;
C.原电池的反应必须是自发的氧化还原反应;
D.铅离子与硫酸根结合成难溶物硫酸铅.
解答 解:A.放电时,电子不进入电解质溶液,电解质溶液中通过离子定向移动形成电流,故A错误;
B.在NaOH溶液中,铝能与NaOH溶液发生氧化还原反应,在该反应中,铝失电子作原电池的负极,而属镁和氢氧化钠溶液不能发生氧化还原反应,故B错误;
C.原电池的反应必须是自发的氧化还原反应,从理论上来讲,任何自发的氧化还原反应均可设计为原电池,故C正确;
D.放电时Pb失电子发生氧化反应,则Pb为负极,电极反应式为Pb+SO42--2e-═PbSO4,故D错误.
故选C.
点评 本题考查原电池工作原理,为高频考点,明确得失电子与电极关系、电极反应式的书写是解本题关键,易错点是电子不能通过电解质溶液以及失电子的电极作负极,试题培养了学生的灵活应用能力.

练习册系列答案
相关题目
11.初中常见的3种元素X、Y和Z的相关信息如下表所示.
请用元素符号或化学式回答下列问题:
(1)Z的元素符号是O.
(2)X的元素原子容易变成X+,其原因是金属性强.
(3)Y的单质与不充足的Z的单质反应,其产物的化学式为CO.
(4)YZ2可与X的氢氧化物发生反应,该反应的化学方程式为CO2+2NaOH=Na2CO3+H2O.
(5)由X、Y、Z三种元素组成的化合物与一定量的稀盐酸混合后的现象为有气体生成,该反应的化学方程式为Na2CO3+2HCl=2NaCl+H2O+CO2↑.
| 元素 | X | Y | Z |
| 相关 信息 | 食盐中存在的 金属元素 | 其一种单质是天然 存在的最硬的物质 | 地壳中含量 最多的元素 |
(1)Z的元素符号是O.
(2)X的元素原子容易变成X+,其原因是金属性强.
(3)Y的单质与不充足的Z的单质反应,其产物的化学式为CO.
(4)YZ2可与X的氢氧化物发生反应,该反应的化学方程式为CO2+2NaOH=Na2CO3+H2O.
(5)由X、Y、Z三种元素组成的化合物与一定量的稀盐酸混合后的现象为有气体生成,该反应的化学方程式为Na2CO3+2HCl=2NaCl+H2O+CO2↑.
18.下列表示化学过程的化学式书写正确的是( )
| A. | 亚硫酸钠溶液显碱性:SO32-+2 H2O?H2SO3+2 OH- | |
| B. | 氯化银投入水中后建立平衡:AgCl (s)?Ag+(aq)+Cl-(aq) | |
| C. | 甲烷的燃烧热为890.3kJ•mol-1,表示甲烷燃烧热的热化学方程式为: CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-890.3kJ•mol-1 | |
| D. | 500℃、30MPa下,将0.5mol N2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,热化学方程式为:N2(g)+3H2(g)$?_{500℃、30MPa}^{催化剂}$ 2NH3(g)△H=-38.6 kJ•mol-1 |
8.下列反应的离子方程式正确的是( )
| A. | 碳酸钙溶于醋酸 CaCO3+2H+═Ca2++CO2↑+H2O | |
| B. | 氯化铁溶液溶解铜 Cu+2Fe3+═Cu2++2Fe2+ | |
| C. | 氯气溶于水 Cl2+H2O═2H++Cl-+ClO- | |
| D. | 氢氧化钠溶液吸收二氧化硫气体 SO2+2OH-═SO42-+H2O |
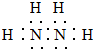 ,其中氮的化合价为-2价.
,其中氮的化合价为-2价.