题目内容
13.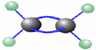 如图是某有机物分子的球棍式模型,其中大球代表碳原子,小球代表氢原子,短棍代表共价键,该有机物的名称是( )
如图是某有机物分子的球棍式模型,其中大球代表碳原子,小球代表氢原子,短棍代表共价键,该有机物的名称是( )| A. | 乙烯 | B. | 乙烷 | C. | 乙醇 | D. | 乙炔 |
分析 根据球棍模型是一种空间填充模型,用来表现化学分子的三维空间分布.在此作图方式中,线代表共价键,可连结以球型表示的原子中心;碳原子形成四个共价键,氢原子形成一个共价键.
解答 解:因球棍模型是一种空间填充模型,用来表现化学分子的三维空间分布,碳原子形成四个共价键,氢原子形成一个共价键,得到有机物的结构简式为CH2=CH2,即为乙烯;
故选A.
点评 本题考查了球棍模型的基本知识,理解碳原子形成四个化学键是解题关键,题目较简单.

练习册系列答案
相关题目
3.已知某溶液中存在较多的SO42-、NO3-则溶液中还可能大量存在的离子组是( )
| A. | Fe3+、AlO2-、Cl- | B. | Na+、NH4+、S2- | C. | H+、Cl-、Fe2+ | D. | Mg2+、Ba2+、Br- |
4.硅单质及其化合物应用十分广泛,下列说法错误的是( )
| A. | 硅胶可用作食品干燥剂 | |
| B. | 二氧化硅可制成石英坩埚 | |
| C. | 单质硅可用于制光导纤维 | |
| D. | 硅酸钠溶液浸泡木材可起到防火作用 |
1.对下面与化学变化相关的图片的说法不正确的是( )
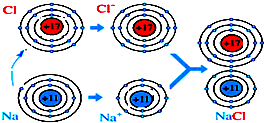

| A. | 上述过程中涉及的反应是氧化还原反应 | |
| B. | 上述过程中金属元素失去电子 | |
| C. | 上述过程中有电子的得失 | |
| D. | 离子间的反应也能形成共价键 |
8.设NA为阿伏加德罗常数,则下列说法正确的是( )
| A. | 22.4 L乙烯中含有的分子数为NA | |
| B. | 0.1 L 0.1 mol/L的CH3COOH溶液中含有的分子数为0.01 Na | |
| C. | 含0.1 mol H2O2的水溶液跟MnO2充分作用,反应过程中转移的电子总数0.1Na | |
| D. | 1 mol HCl气体中的粒子数与0.5 mol/L盐酸中溶质粒子数相等 |
18.某原电池的总反应是Zn+Cu2+=Zn2++Cu,该原电池的正确组成是( )
| 选项 | A | B | C | D |
| 正极材料 | Zn | Cu | Zn | Cu |
| 负极材料 | Cu | Zn | Cu | Zn |
| 电解质溶液 | CuCl2 | CuSO4 | ZnSO4 | ZnCl2 |
| A. | A | B. | B | C. | C | D. | D |
5.硫代硫酸钠(Na2S2O3)与稀H2SO4溶液时发生如下反应:Na2S2O3+H2SO4=Na2 SO4+SO2+S↓+H2O 下列反应速率最大的是( )
| A. | 0.1mol/L Na2S2O3和0.1mol/L H2SO4溶液各5mL,加水5mL,反应温度10℃ | |
| B. | 0.1mol/L Na2S2O3和0.1mol/L H2SO4溶液各5mL,加水10mL,反应温度10℃ | |
| C. | 0.1mol/L Na2S2O3和0.1mol/L H2SO4溶液各5mL,加水10mL,反应温度30℃ | |
| D. | 0.2mol/L Na2S2O3和0.1mol/L H2SO4溶液各5mL,加水10mL,反应温度30℃ |
2.下列各表中的数字代表的时原子序数,表中数字所表示的元素与它们在元素周期表中的位置相符的是( )
| A. |
| B. |
| C. |
| D. |
|