题目内容
15.下列关于砷(33As)元素的叙述中,不正确的是( )| A. | 在AsCl3分子构型为三角锥形 | |
| B. | Na3AsO4溶液的pH大于7 | |
| C. | 砷的氢化物的化学式为AsH3,它的沸点比NH3低 | |
| D. | 砷元素的相对原子质量为75,由此可知砷原子核内必有42个中子 |
分析 A.根据价层电子对互斥理论确定其空间构型,价层电子对个数=σ 键+孤电子对个数;
B.强碱弱酸盐溶液水解呈碱性;
C.从是否形成氢键的角度分析,形成分子间氢键沸点高;
D.元素的相对原子质量=各同位素的质量数×各同位素原子的丰度,砷元素的相对原子质量为75是平均计算值,不能确定某一Se原子的质量数.
解答 解:A.AsCl3分子中,价层电子对数=3+$\frac{1}{2}$(5-3×1)=4,且含有一个孤电子对,所以其空间构型是三角锥型,故A正确;
B.Na3AsO4为强碱弱酸盐,AsO43-水解溶液呈碱性,故B正确;
C.砷的氢化物的化学式为AsH3,N原子半径较小,电负性较大,对应的NH3分子间能形成氢键,沸点较高,而As电负性小,半径大,分子间不能形成氢键,沸点较低,故C正确;
D.元素的相对原子质量=各同位素的质量数×各同位素原子的丰度,75是砷元素的各同位素的平均计算值,不能确定某一Se原子的质量数,故D错误;
故选:D.
点评 本题以砷(33As)元素为载体考查分子构型、盐类的水解、氢键、相对原子质量等知识,题目难度中等,侧重对基础知识的巩固利用,注意价层电子对互斥理论应用高频考点.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
5.下列有关说法正确的是( )
| A. | 含有醛基的物质一定是醛 | |
| B. | 含醛基的物质能发生银镜反应,但不能使酸性KMnO4溶液褪色 | |
| C. | 醛类物质常温常压下都为液体或固体 | |
| D. | 醛与H2发生的加成反应也是还原反应 |
6.盐城地区进入冬季,早上经常出现大雾天气.请问雾属于下列哪一种分散系( )
| A. | 溶液 | B. | 悬浊液 | C. | 胶体 | D. | 乳浊液 |
3.下列各分子式只表示一种纯净物的是( )
| A. | C2H2Br2 | B. | C3H8 | C. | C4H10 | D. | C5H10 |
10.为了除去蛋白质溶液中混入的少量氯化钠,可以采用的方法是( )
| A. | 过滤 | B. | 盐析 | ||
| C. | 渗析 | D. | 加入AgNO3溶液,过滤 |
20.各种能量可以相互转化.下述能量未必由化学能转化而来的是( )
| A. | 电解铝所需的电能 | B. | 人的体能 | ||
| C. | 化学电池的电能 | D. | 燃油汽车的动能 |
7.从海带中提取碘的实验过程中,涉及到下列操作,其中正确的是( )
| A. | 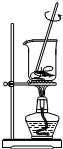 将海带灼烧成灰 | B. | 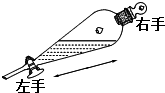 萃取振摇 | ||
| C. | 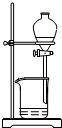 放出碘的苯溶液 | D. | 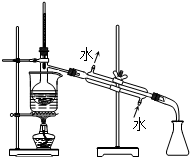 分离碘并回收苯 |
5.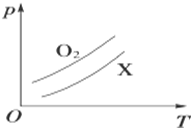 如图表示1g O2与1g X气体在相同容积的密闭容器中压强(p)与温度(T)的关系,则X气体不可能是( )
如图表示1g O2与1g X气体在相同容积的密闭容器中压强(p)与温度(T)的关系,则X气体不可能是( )
 如图表示1g O2与1g X气体在相同容积的密闭容器中压强(p)与温度(T)的关系,则X气体不可能是( )
如图表示1g O2与1g X气体在相同容积的密闭容器中压强(p)与温度(T)的关系,则X气体不可能是( )| A. | C2H6 | B. | CH4 | C. | CO2 | D. | SO2 |
 .
.