题目内容
【题目】高纯氧化铁是现代电子工业的重要材料.以下是用硫酸厂产生的烧渣![]() 主要成分为
主要成分为![]() 、
、![]() 、FeO、
、FeO、![]() 为原料制备高纯氧化铁
为原料制备高纯氧化铁![]() 软磁
软磁![]() 的生产流程示意图,下列说法不正确的是
的生产流程示意图,下列说法不正确的是![]()
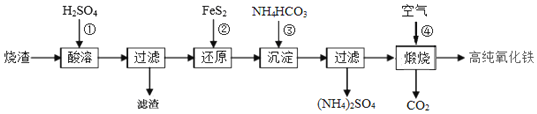
A.酸浸时,常需将烧渣粉碎、并加入过量![]() ,其目的是提铁元素的浸出率,同时抑制铁离子的水解
,其目的是提铁元素的浸出率,同时抑制铁离子的水解
B.加入![]() 时,发生反应
时,发生反应![]() 的离子方程式为
的离子方程式为![]()
C.加入![]() 为了生成
为了生成![]() ,检验
,检验![]() 是否洗涤干净的方法是取最后一次洗涤液少量放入试管,滴加盐酸酸化的氯化钡溶液,若无沉淀生成,说明洗涤干净
是否洗涤干净的方法是取最后一次洗涤液少量放入试管,滴加盐酸酸化的氯化钡溶液,若无沉淀生成,说明洗涤干净
D.煅烧时空气中的氧气作氧化剂,所以用氯气代替空气也可得到高纯氧化铁
【答案】D
【解析】
根据题中生产流程示意图可知,本题考查工业制备高纯氧化铁,运用铁及其化合物的性质分析。
![]() 烧渣
烧渣![]() 主要成分为
主要成分为![]() 、
、![]() 、FeO、
、FeO、![]() ,酸浸时与稀硫酸反应得到
,酸浸时与稀硫酸反应得到![]() 、
、![]() ,酸浸时,常需将烧渣粉碎,通过增大接触面积,提高铁元素的浸出率,因亚铁离子、铁离子都易水解呈酸性,通过加入过量
,酸浸时,常需将烧渣粉碎,通过增大接触面积,提高铁元素的浸出率,因亚铁离子、铁离子都易水解呈酸性,通过加入过量![]() ,抑制铁离子的水解,故A正确;
,抑制铁离子的水解,故A正确;
B.滤液中加入![]() 将
将![]() 还原为
还原为![]() ,
,![]() 价的硫被氧化成
价的硫被氧化成![]() 价的硫,
价的硫,![]() ,失去
,失去![]() ,
,![]() ,得到
,得到![]() ,最小公倍数为14,根据得失电子守恒、原子守恒和电荷守恒,离子反应方程式为:
,最小公倍数为14,根据得失电子守恒、原子守恒和电荷守恒,离子反应方程式为:![]() ,故B正确;
,故B正确;
C.![]() 能和硫酸反应生成硫酸铵和二氧化碳,同时能调节溶液的pH,使
能和硫酸反应生成硫酸铵和二氧化碳,同时能调节溶液的pH,使![]() 全部转化为
全部转化为![]() ,过滤得碳酸亚铁,滤液中有硫酸铵,所以检验
,过滤得碳酸亚铁,滤液中有硫酸铵,所以检验![]() 是否洗净,就是检验洗涤滤液中是否有硫酸根离子,所以操作为取最后一次洗涤滤液,滴加盐酸酸化排除碳酸根离子的干扰,滴加盐酸酸化的氯化钡溶液,若无沉淀生成,说明洗涤干净,故C正确;
是否洗净,就是检验洗涤滤液中是否有硫酸根离子,所以操作为取最后一次洗涤滤液,滴加盐酸酸化排除碳酸根离子的干扰,滴加盐酸酸化的氯化钡溶液,若无沉淀生成,说明洗涤干净,故C正确;
D.煅烧时空气中的氧气作氧化剂,用氯气代替空气会生成氯化铁,不能得到高纯氧化铁,故D错误;
答案选D。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】电解质水溶液中存在电离平衡、水解平衡、溶解平衡等,请回答下列问题。
(1)已知部分弱酸的电离常数如下表:
弱酸 | CH3COOH | HCN | H2CO3 |
电离常数(室温) | Ka= 1.8×10-5 | Ka=4.3×10-10 | Ka1=5.0×10-7 Ka2=5.6×10-11 |
①0.1mol/L NaCN溶液和0.1mol/L NaHCO3溶液中,c(CN-)______c(HCO3- )(填“>”、“<”或“=”)。
②将浓度均为0.1mol/L的CH3COONa、NaCN、NaHCO3和Na2CO3溶液分别稀释100倍,pH变化最小的是__________。
③将少量CO2通入NaCN溶液,反应的离子方程式是_____。
④室温下,—定浓度的CH3COONa溶液pH=9,用离子方程式表示溶液呈碱性的原因是_____,溶液中c(CH3COO-)/c(CH3COOH) =___________。
⑤室温下,某溶液中存在着CH3COOH(aq)+HCO3-( aq)CH3COO-(aq) +H2CO3(aq),该反应的平衡常数K =___________。
⑥室温下,pH =4的CH3COOH与pH =10的CH3COONa溶液中,由水电离出的c(H+)之比_______。
(2)已知室温下Cu(OH)2的Ksp=2×10-20,又知室温下某CuSO4溶液中c(Cu2+)=0.02mol/L,如果要生成Cu(OH)2沉淀,则应调整溶液的pH大于___________
