题目内容
现有金属单质A、B、C和气体甲、乙、丙及物质D、E、F、G、H,它们之间能发生如图反应(图中有些反应的产物和反应的条件没有全部标出):

(1)写出下列物质的化学式:A 、B 、C 、F 、乙
(2)写出下列反应化学方程式:
反应① 反应⑤ .

(1)写出下列物质的化学式:A
(2)写出下列反应化学方程式:
反应①
考点:无机物的推断
专题:推断题
分析:金属单质A的与水反应生成气体和物质D,D与金属B反应,则A应为Na,与水反应生成的气体甲为H2,C为NaOH,黄绿色气体乙为Cl2,则丙为HCl,E为盐酸;
D为NaOH,与金属B反应生成氢气,则B为Al;盐酸与金属C反应生成F,F可被氯气氧化,则金属C为变价金属Fe,则F为FeCl2 ,G为FeCl3,结合物质的性质解答该题.
D为NaOH,与金属B反应生成氢气,则B为Al;盐酸与金属C反应生成F,F可被氯气氧化,则金属C为变价金属Fe,则F为FeCl2 ,G为FeCl3,结合物质的性质解答该题.
解答:
解:金属单质A的与水反应生成气体和物质D,D与金属B反应,则A应为Na,与水反应生成的气体甲为H2,C为NaOH,黄绿色气体乙为Cl2,则丙为HCl,E为盐酸;
D为NaOH,与金属B反应生成氢气,则B为Al;盐酸与金属C反应生成F,F可被氯气氧化,则金属C为变价金属Fe,则F为FeCl2 ,G为FeCl3,
(1)由以上分析可知A为Na,B为Al,C为Fe,F为FeCl2,乙为Cl2,故答案为:Na;Al;Fe;FeCl2;Cl2;
(2)反应①为2Na+2H2O=2NaOH+H2↑,反应③为2FeCl2+Cl2═2FeCl3,故答案为:2Na+2H2O=2NaOH+H2↑;2FeCl2+Cl2═2FeCl3.
D为NaOH,与金属B反应生成氢气,则B为Al;盐酸与金属C反应生成F,F可被氯气氧化,则金属C为变价金属Fe,则F为FeCl2 ,G为FeCl3,
(1)由以上分析可知A为Na,B为Al,C为Fe,F为FeCl2,乙为Cl2,故答案为:Na;Al;Fe;FeCl2;Cl2;
(2)反应①为2Na+2H2O=2NaOH+H2↑,反应③为2FeCl2+Cl2═2FeCl3,故答案为:2Na+2H2O=2NaOH+H2↑;2FeCl2+Cl2═2FeCl3.
点评:本题以无机框图题的形式考查Na、Al、Fe、Cl等元素单质及其化合物之间的相互转化关系、化学用语的书写等,为高频考点,侧重于学生的分析能力和元素化合物知识的综合运用的考查,难度中等,注意把握物质之间转化的特点,尤其是物质反应的典型现象,注意基础知识的掌握.

练习册系列答案
相关题目
下列分离和提纯的实验,所选用的方法和仪器不正确的是( )
| 序号 | A | B | C | D |
| 实验目的 | 食盐水与泥沙分离 | 制取蒸馏水 | 分离水和植物油 | 从浓食盐水中 得到氯化钠晶体 |
| 分离方法 | 萃取 | 蒸馏 | 分液 | 蒸发 |
| 选用仪器 | 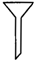 | 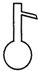 | 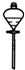 |  |
| A、A | B、B | C、C | D、D |
用惰性电极电解饱和Na2CO3溶液,若保持温度不变,则一段时间后( )
| A、溶液的酸性增强 | ||
B、c(Na+)与c(CO
| ||
| C、溶液浓度变大,有晶体析出 | ||
| D、溶液浓度不变,有晶体析出 |
北京奥运会“祥云”火炬所用燃料的主要成分是丙烷,下列有关丙烷的叙述错误的是( )
| A、分子中的3个碳原子在一条直线上 |
| B、在光照条件下能和氯气发生取代反应 |
| C、充分燃烧的产物是水和二氧化碳 |
| D、丙烷和丁烷互为同系物 |
衡量一个国家化学工业发展水平标志的是下列哪一种物质的产量( )
| A、钢铁 |
| B、石油和煤 |
| C、乙烯 |
| D、CO2的排放量 |
乙炔在一定条件下与水发生加成反应(工业上曾利用该反应制乙醛,称乙炔水化法制乙醛),其过程如下:CH≡CH+H-OH→[H2C=CH-OH]→CH3CHO.已知H2C=CH-OH在常温下为液体且很不稳定,很容易转化为稳定的CH3CHO.然而,2002年美国《科学》杂志报道:外太空的某一星球上含有大量的H2C=CH-OH.从化学平衡的角度预测该星球的温度应该是( )
| A、常温 | B、较高温度 |
| C、较低温度 | D、无法判断温度高低 |
在相同状况下将镁、铝、铁分别投入质量相等且足量的稀硫酸中,反应结束后,三种溶液的质量仍相等,则投入镁、铝、铁三种金属的质量关系正确的是( )
| A、Mg>Al>Fe |
| B、Al>Fe>Mg |
| C、Al>Mg>Fe |
| D、Fe>Mg>Al |