题目内容
10.b g某金属与足量的稀硫酸反应,生成该金属的三价正盐和a g氢气.该金属的相对原子质量为( )| A. | $\frac{2b}{a}$ | B. | $\frac{3b}{a}$ | C. | $\frac{2b}{2a}$ | D. | $\frac{a}{3b}$ |
分析 根据金属的化合价和氢气的物质的量求出金属的物质的量,进而求出金属的摩尔质量,再利用摩尔质量与相对原子质量的关系来解答.
解答 解:ag氢气的物质的量为:n(H2)=$\frac{ag}{2g/mol}$=0.5amol,
设金属为A,bg金属的物质的量为x,
根据反应方程式:2A+3H2SO4=A2(SO4)3+3H2↑
2 3
x 0.5amol
则:$\frac{2}{x}=\frac{3}{0.5a}$
解得:x=$\frac{a}{3}$mol,
M(金属)=$\frac{m}{n}$=$\frac{bg}{\frac{a}{3}mol}$=$\frac{3b}{a}$g/mol,
由金属的摩尔质量与其相对原子质量在数值上相等,即金属的相对原子质量为 $\frac{3b}{a}$,
故选B.
点评 本题考查相对原子质量及其计算,做题注意从金属的化合价计算金属的物质的量,进而计算相对原子质量.

练习册系列答案
 开心蛙状元作业系列答案
开心蛙状元作业系列答案 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案 一课一练一本通系列答案
一课一练一本通系列答案 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案
相关题目
1.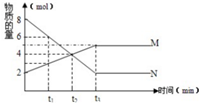 在一定温度下,容器内某反应中M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )
在一定温度下,容器内某反应中M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )
 在一定温度下,容器内某反应中M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )
在一定温度下,容器内某反应中M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )| A. | t3时,正反应速率大于逆反应速率 | |
| B. | t2时,正逆反应速率相等,反应达到平衡状态 | |
| C. | 化学方程式为:2M=N | |
| D. | t1时,N的浓度是M浓度的2倍 |
18.下列说法正确的是( )


| A. | 用甘氨酸(H2NCH2COOH)和丙氨酸(CH3CHNH2COOH)缩合,最多可形成4种二肽 | |
| B. | 在酸性条件下,CH3CO18OC2H5水解的产物是CH3CO18OH和C2H5OH | |
| C. | 实验室用如图装置证明酸性:醋酸>碳酸>苯酚,①中放入浓醋酸,②中放入CaCO3,③中放入C6H5ONa溶液 | |
| D. | 实验室用如图装置证明乙炔具有还原性,①中放入H2O,②中放入电石,③中放入KMnO4溶液 |
5.相同物质的量浓度的NaX、NaY、NaZ三种盐溶液的pH分别为7、8、9,则相同物质的量浓度的HX、HY、HZ的酸性强弱顺序为( )
| A. | HX、HY、HZ | B. | HZ、HY、HX | C. | HX、HZ、HY | D. | HZ、HY、HX |
2.(1)已知25℃时,Ksp(BaSO4)=1×10-10,Ksp(BaCO3)=2.5×10-9将浓度均为0.1mol•L-1的BaCl2溶液与Na2SO4溶液等体积混合,充分搅拌后过滤,滤液中C(Ba2+)=1×10-5mol•L-1.取100mL滤液与100mL 2mol•L-1的Na2SO4溶液混合,混合液中C(Ba2+)=1×10-10mol•L-1
(2)25℃醋酸的电离常数Ka=1.7×10-5mol•L-1 计算此温度下CH3COO-的水解平衡常数Kh=5.9×10-10mol•L-1.
| 阳离子 | Na+,Ba2+,NH4+ |
| 阴离子 | CH3COO-,Cl-,OH-,SO42- |
9.化学是一门实用性很强的科学,与社会、环境等密切相关.下列说法错误的是( )
| A. | “静电除尘”、“燃煤固硫”、“汽车尾气催化净化”都能提高空气质量 | |
| B. | 用NH4Cl浓溶液除铁锈,因为NH4 Cl水解显酸性 | |
| C. | 用CO2合成聚碳酸酯可降解塑料,实现“碳”的循环利用 | |
| D. | 在食品袋中放入CaCl2•6H2O,可防止食物受潮 |
6.常温下,向浓HNO3中加入下列物质,反应最快、现象最明显的是( )
| A. | Al | B. | Cu | C. | Fe | D. | C |
7.下列个组物质中互为同系物的是( )
| A. | CH2=CH2、 | B. | CH4、CH3CH2CH3 | ||
| C. | C2H2、C6H6 | D. | CH3-O-CH3、CH3-OH |
 ,请回答下列问题.
,请回答下列问题. .
.