题目内容
A、B、C 三种物质有如图所示转化关系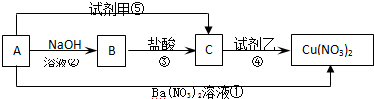
(1)根据上述转化关系,写出下列物质化学式A B C 试剂甲 试剂乙
(2)写出上述各步反应离子方程式
1
2
3
4
5 .

(1)根据上述转化关系,写出下列物质化学式A
(2)写出上述各步反应离子方程式
1
2
3
4
5
考点:无机物的推断
专题:推断题
分析:由转化关系可知A可与硝酸钡反应生成硝酸铜,则A应为CuSO4,由此可知B为Cu(OH)2,C为CuCl2,甲为BaCl2,乙为AgNO3,结合对应物质的性质解答该题.
解答:
解:(1)由转化关系可知A可与硝酸钡反应生成硝酸铜,则A应为CuSO4,由此可知B为Cu(OH)2,C为CuCl2,甲为BaCl2,乙为AgNO3,
故答案为:CuSO4;Cu(OH)2;CuCl2;BaCl2;AgNO3;
(2)①为CuSO4与硝酸钡的反应,离子方程式为SO42-+Ba2+=BaSO4↓,
②为CuSO4和NaOH的反应,离子方程式为Cu2++2OH-=Cu(OH)2↓,
③为Cu(OH)2和盐酸的反应,离子方程式为Cu(OH)2+2H+=Cu2++2H2O,
④为CuCl2和AgNO3的反应,离子方程式为Ag++Cl-=AgCl↓,
⑤为CuSO4和BaCl2的反应,离子方程式为SO42-+Ba2+=BaSO4↓,
故答案为:SO42-+Ba2+=BaSO4↓;Cu2++2OH-=Cu(OH)2↓;Cu(OH)2+2H+=Cu2++2H2O;Ag++Cl-=AgCl↓;SO42-+Ba2+=BaSO4↓.
故答案为:CuSO4;Cu(OH)2;CuCl2;BaCl2;AgNO3;
(2)①为CuSO4与硝酸钡的反应,离子方程式为SO42-+Ba2+=BaSO4↓,
②为CuSO4和NaOH的反应,离子方程式为Cu2++2OH-=Cu(OH)2↓,
③为Cu(OH)2和盐酸的反应,离子方程式为Cu(OH)2+2H+=Cu2++2H2O,
④为CuCl2和AgNO3的反应,离子方程式为Ag++Cl-=AgCl↓,
⑤为CuSO4和BaCl2的反应,离子方程式为SO42-+Ba2+=BaSO4↓,
故答案为:SO42-+Ba2+=BaSO4↓;Cu2++2OH-=Cu(OH)2↓;Cu(OH)2+2H+=Cu2++2H2O;Ag++Cl-=AgCl↓;SO42-+Ba2+=BaSO4↓.
点评:本题考查无机物推断,根据复分解反应确定A是关键,然后结合推出的物质题中的转换关系推导剩余的物质,最后进行验证即可,难点不大.

练习册系列答案
相关题目
某同学通过系列实验探究Cu及其化合物的性质,操作正确且能达到的目的是( )
| A、将铜粉与硫粉混合均匀加热以制取CuS |
| B、向Cu与过量浓硫酸反应后的试管中加水以观察CuSO4溶液的颜色 |
| C、向CuSO4溶液中加入过量的NaOH,过滤洗涤并收集沉淀充分灼烧以制取CuO |
| D、在淀粉溶液中加入适量稀H2SO4微热,再加少量新制Cu(OH)2悬溶液并加热,产生红色沉淀 |
在xR2++yH++O2=mR3++nH2O的离子方程式中,对系数m和R3+的判断正确的是( )
| A、m=2,R3+是还原产物 |
| B、m=6,R3+是氧化产物 |
| C、m=4,R3+是氧化产物 |
| D、m=8,R3+是还原产物 |