题目内容
某同学通过系列实验探究Cu及其化合物的性质,操作正确且能达到的目的是( )
| A、将铜粉与硫粉混合均匀加热以制取CuS |
| B、向Cu与过量浓硫酸反应后的试管中加水以观察CuSO4溶液的颜色 |
| C、向CuSO4溶液中加入过量的NaOH,过滤洗涤并收集沉淀充分灼烧以制取CuO |
| D、在淀粉溶液中加入适量稀H2SO4微热,再加少量新制Cu(OH)2悬溶液并加热,产生红色沉淀 |
考点:铜金属及其重要化合物的主要性质
专题:
分析:A.由于硫的氧化性弱,所以只能将铜氧化成一价;
B.常温下铜与浓硫酸不反应;
C.向CuSO4溶液中加入过量的NaOH产生氢氧化铜的沉淀,过滤洗涤并灼烧氢氧化铜分解生成氧化铜;
D.葡萄糖和新制氢氧化铜反应必须在碱性条件下进行.
B.常温下铜与浓硫酸不反应;
C.向CuSO4溶液中加入过量的NaOH产生氢氧化铜的沉淀,过滤洗涤并灼烧氢氧化铜分解生成氧化铜;
D.葡萄糖和新制氢氧化铜反应必须在碱性条件下进行.
解答:
解:A.由于硫的氧化性弱,所以只能将铜氧化成一价,故A错误;
B.常温下铜与浓硫酸不反应,因此观察不到现象,故B错误;
C.向CuSO4溶液中加入过量的NaOH产生氢氧化铜的沉淀,过滤洗涤并灼烧氢氧化铜分解生成氧化铜,故C正确;
D.葡萄糖和新制氢氧化铜反应必须在碱性条件下进行,该反应在淀粉溶液中加入适量稀硫酸微热,在酸性条件下进行,所以实验不成功,不能说明淀粉没有水解,故D错误;
故选C.
B.常温下铜与浓硫酸不反应,因此观察不到现象,故B错误;
C.向CuSO4溶液中加入过量的NaOH产生氢氧化铜的沉淀,过滤洗涤并灼烧氢氧化铜分解生成氧化铜,故C正确;
D.葡萄糖和新制氢氧化铜反应必须在碱性条件下进行,该反应在淀粉溶液中加入适量稀硫酸微热,在酸性条件下进行,所以实验不成功,不能说明淀粉没有水解,故D错误;
故选C.
点评:本题考查了铜及其化合物的性质,关键是反应条件的选择,题目难度不大.

练习册系列答案
相关题目
下列解释实验事实的方程式不正确的是( )
| A、可用氯气进行自来水的杀菌消毒:Cl2+H2O═HCl+HClO |
| B、将“NO2球”浸泡在热水中,颜色变深:2NO2(g)═N2O4(g)△H<0 |
| C、在刻制印刷电路板时,用FeCl3溶液腐蚀铜箔:2Fe3++3Cu═2Fe+3Cu2+ |
| D、在KNO3和稀硫酸混合液中,铜片溶解:3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O |
水是生命之源,下列关于水的说法正确的是( )
| A、海水淡化的方法主要有蒸馏法、电渗析法、离子交换法等 |
| B、某温度下,pH=6的蒸馏水显酸性 |
| C、氯气有毒,因而自来水的杀菌消毒一定不能使用氯气 |
| D、明矾可用于水的净化与杀菌消毒 |
CuI是一种不溶于水的白色固体,它可以由反应:2Cu2++4I-=2CuI↓+I2而得到.现以石墨为阴极,以Cu为阳极电解KI溶液,通电前向电解液中加入少量酚酞和淀粉溶液.电解开始不久,阴极区溶液呈红色,而阳极区溶液呈蓝色.对阳极区溶液呈蓝色的正确解释是( )
| A、2 I--2e-=I2 碘遇淀粉变蓝 |
| B、Cu-2e-=Cu2+ Cu2+ 显蓝色 |
| C、2Cu+4I--4e-=2CuI↓+I2 碘遇淀粉变蓝 |
| D、4OH--4e-=2H2O+O2 O2将I-氧化为I2,碘遇淀粉变蓝 |
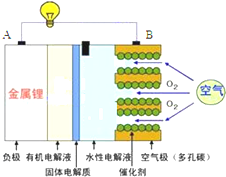 锂空气电池是一种用锂作负极,以空气中的氧气作为正极反应物的电池.其比锂离子电池具有更高的能量密度,具有很广阔的应用前景.其工作原理如图,下列说法中正确的是( )
锂空气电池是一种用锂作负极,以空气中的氧气作为正极反应物的电池.其比锂离子电池具有更高的能量密度,具有很广阔的应用前景.其工作原理如图,下列说法中正确的是( )| A、电池工作时电子从A流向B,再由B经电池内 部流向A,形成闭合回路 |
| B、电池总反应为4Li+O2=2Li2O(Li2O不溶于水) |
| C、该电池只需更换负极材料和水性电解液,可以长期供电 |
| D、用该电池电解精炼铜,理论上消耗7g锂,可以得到64g铜 |
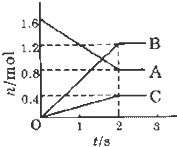 某温度下,在体积为5L的容器中,A、B、C三种物质物质的量随着时间变化的关系如图所示,则该反应的化学方程式为
某温度下,在体积为5L的容器中,A、B、C三种物质物质的量随着时间变化的关系如图所示,则该反应的化学方程式为