题目内容
6.下列叙述正确的是( )| A. | 含2molH2SO4的浓硫酸与足量铜反应生成1molSO2 | |
| B. | 硫粉在过量的氧气中燃烧可以生成SO3 | |
| C. | 铜与稀硝酸反应生成0.5molNO气体,则转移电子数为NA | |
| D. | 可用品红溶液或酸性KMnO4溶液鉴别 CO2和SO2,不可用澄清石灰水鉴别 CO2和SO2 |
分析 A、根据铜与稀硫酸不发生反应分析;
B、硫在氧气中燃烧生成二氧化硫;
C、生成1mol的一氧化氮转移电子数为3mol;
D、SO2具有还原性,二氧化硫也能使澄清石灰水变浑浊.
解答 解:A、根据铜与稀硫酸不发生,所以2molH2SO4的浓硫酸没有完全反应,故A错误;
B、硫在氧气中燃烧生成二氧化硫,而不是三氧化硫,故B错误;
C、生成1mol的一氧化氮转移电子数为3mol,所以生成0.5molNO气体,则转移电子数为1.5NA,故C错误;
D、SO2具有还原性,二氧化硫也能使澄清石灰水变浑浊,所以可用品红溶液或酸性KMnO4溶液鉴别 CO2和SO2,不可用澄清石灰水鉴别 CO2和SO2,故D正确;
故选D.
点评 本题考查了阿伏伽德罗常数的计算及判断,题目难度不大,稀硫酸与铜不反应,熟练掌握物质的量与阿伏伽德罗常数之间的转化关系.

练习册系列答案
 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案
相关题目
14.加成反应也是有机化学中的一类重要的反应类型,下列物质各组物质中不能全部发生加成反应的是( )
| A. | 乙烷、乙烯 | B. | 乙烯、乙炔 | C. | 氯乙烯、溴乙烯 | D. | 苯、2-丁烯 |
1.表为截取的元素周期表前4周期的一部分,且X、Y、Z、R和W均为主族元素.下列说法正确的是( )
| X | ||
| Y | Z | R |
| W |
| A. | Z的氧化物与X单质不可能发生置换反应 | |
| B. | X、Z原子序数可能相差18 | |
| C. | Z可能是氯元素 | |
| D. | 五种元素的原子最外层电子数一定都大于2 |
18.下列说法不正确的是( )
| A. | 化学反应中一定有化学键断裂,同时也有化学键形成 | |
| B. | 只含共价键的物质一定是共价化合物 | |
| C. | 离子化合物一定含有离子键,可能含有共价键 | |
| D. | 金属元素和非金属元素形成的化合物不一定是离子化合物 |
15.X、Y、Z、R均为短周期元素,X、Y、R同周期,其中R的质子数最大;X、Z同主族.X的原子结构示意图为: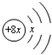 ,Y的原子半径在短周期中最大,Y与R最外层电子数之比为1:7.下列叙述正确的是( )
,Y的原子半径在短周期中最大,Y与R最外层电子数之比为1:7.下列叙述正确的是( )
 ,Y的原子半径在短周期中最大,Y与R最外层电子数之比为1:7.下列叙述正确的是( )
,Y的原子半径在短周期中最大,Y与R最外层电子数之比为1:7.下列叙述正确的是( )| A. | 对应氢化物的沸点:R>Z>X | |
| B. | Y、Z形成的化合物中只有离子键 | |
| C. | 离子半径:X>Z>Y | |
| D. | Z与X、Y与R形成化合物的晶体类型相同 |
16.下列反应中属于加成反应的是( )
| A. | CH2=CH2+HCl→CH3CH2Cl | B. | CH4+Cl2$\stackrel{光照}{→}$CH3Cl+HCl | ||
| C. | 2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O | D. | 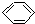 +HO-NO2 $→_{60℃}^{浓硫酸}$ +HO-NO2 $→_{60℃}^{浓硫酸}$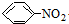 +H2O +H2O |
 现有一套电化学装置,如图所示,E 为沾有 Na2SO4溶液的滤纸,并加入几滴酚酞.A、B分别为Pt片,压在滤纸两端,R、S为电源的电极.M、N是用多微孔的 Ni 制成的电极材料,它在碱性溶液中可以视为惰性电极.G为电流计,K为开关.C、D和电解池中都充满浓KOH溶液.若在滤纸中央点上一滴紫色的 KMnO4溶液,断开K,接通外电源一段时间后,C、D中有气体产生.
现有一套电化学装置,如图所示,E 为沾有 Na2SO4溶液的滤纸,并加入几滴酚酞.A、B分别为Pt片,压在滤纸两端,R、S为电源的电极.M、N是用多微孔的 Ni 制成的电极材料,它在碱性溶液中可以视为惰性电极.G为电流计,K为开关.C、D和电解池中都充满浓KOH溶液.若在滤纸中央点上一滴紫色的 KMnO4溶液,断开K,接通外电源一段时间后,C、D中有气体产生.