题目内容
电解之前食盐水需要精制,除去粗盐中Ca2+,Mg2+,SO42-的等杂质离子,使用的试剂有:①NaOH ②BaCl2 ③HCl ④Na2CO3,其加入的顺序合理的是( )
| A、①③④② | B、①②④③ |
| C、③②④① | D、①②③④ |
考点:粗盐提纯
专题:化学实验基本操作
分析:SO42-、Ca2+、Mg2+离子分别转化为硫酸钡、碳酸钙、氢氧化镁沉淀而除去,以及根据不能产生新杂质的要求排序,前面加入的过量溶液应用后加入的溶液除去,最后加入适量的盐酸溶液.
解答:
解:SO42-、Ca2+、Mg2+等分别与BaCl2溶液、Na2CO3溶液、NaOH溶液反应生成沉淀,可再通过过滤除去,Na2CO3溶液能除去过量的BaCl2溶液,盐酸能除去过量的Na2CO3溶液和NaOH溶液,所以应先加②BaCl2溶液再加④Na2CO3溶液,最后加入④盐酸,氢氧化钠溶液加在过滤之前即可,所以正确顺序为:②④①③或①②④③,
故选B.
故选B.
点评:本题主要考查粗盐提纯的步骤及注意事项,题目难度不大,注意掌握除杂试剂的选择及加入试剂的先后顺序,试题培养了学生灵活应用所学知识的能力.

练习册系列答案
相关题目
在某容积一定的密闭容器中,可逆反应:A(g)+B(g)?XC(g);△H<0符合图象(Ⅰ)所示关系,由此推断对图象(Ⅱ)的正确说法是( )


| A、P3>P4,y轴表示A的转化率 |
| B、P3>P4,y轴表示B的质量分数 |
| C、P3>P4,y轴表示混合气体密度 |
| D、P3>P4,y轴表示混合气体的平均式量 |
向浑浊的水中加入适量的明矾[KAl(SO4)2?12H2O]并搅拌以后,水便由浑浊变得澄清.在此过程中发生的主要变化( )
| A、是纯化学变化 |
| B、是纯物理变化 |
| C、既是物理变化又是化学变化 |
| D、不能确定是化学变化还是物理变化 |
四种不同比例H2与CO混合气体VL,它们的平均式量分别为4、8、12、16,若分别完全燃烧则需同温同压下的氧气的体积比是( )
| A、1:1:1 | ||||||||
| B、1:2:3:4 | ||||||||
| C、4:3:2:1 | ||||||||
D、
|
对于反应2SO2(g)+O2(g)?2SO3(g),能增大正反应速率且提高O2的转化率的措施是( )
| A、移去部分SO3 |
| B、降低体系温度 |
| C、通入大量O2 |
| D、通入大量SO2 |
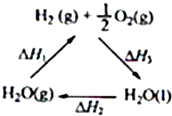 某科学家利用二氧化铈(CeO2)在太阳能作用下将H2O、CO2转变成H2、CO.其过程如下:
某科学家利用二氧化铈(CeO2)在太阳能作用下将H2O、CO2转变成H2、CO.其过程如下:mCeO2
| 太阳能 |
| ① |
(m-x)CeO2?xCe+xH2O+xCO2
| 900℃ |
| ② |
下列说法不正确的是( )
| A、该过程中CeO2没有消耗 | ||
| B、该过程实现了太阳能向化学能的转化 | ||
| C、图中△H1=△H2+△H3 | ||
D、H2(g)+
|