题目内容
10.下列说法错误的是( )| A. | SiO2是难溶于水的酸性氧化物 | |
| B. | 高温下SiO2与碳酸盐反应生成CO2 | |
| C. | SiO2不能与任何酸反应 | |
| D. | 碳化硅(SiC)具有金刚石的结构,硬度很大 |
分析 A.依据二氧化硅难溶于水的性质解答;
B.二氧化硅高温与碳酸盐反应生成硅酸盐和二氧化碳;
C.二氧化硅与氢氟酸反应生成四氟化硅和水;
D.碳化硅与金刚石都是原子晶体,依据原子晶体性质解答.
解答 解:A.二氧化硅为酸性氧化物,难溶于水,故A正确;
B.二氧化硅高温与碳酸盐反应生成硅酸盐和二氧化碳,故B正确;
C.二氧化硅与氢氟酸反应生成四氟化硅和水,故C错误;
D.碳化硅与金刚石都是原子晶体,具有相似的结构,硬度很大,故D正确;
故选:C.
点评 本题考查元素化合物知识,熟悉硅及其化合物性质是解题关键,注意二氧化硅常温下就能够与氢氟酸反应,题目难度不大.

练习册系列答案
相关题目
18.恒温下,在容积为2L的恒容密闭容器中发生反应:2SO2(g)+O2(g)?2SO3(g)△H<0,n(SO2)随时间变化关系如表:
下列说法正确的是( )
| 时间/m i n | 0 | 1 | 2 | 3 | 4 | 5 |
| n(SO2)/mol | 0.2 | 0.16 | 0.13 | 0.11 | 0.08 | 0.08 |
| A. | 当容器中气体的密度不变时,该反应达到平衡状态 | |
| B. | 用SO3表示0~4 min内该反应的平均速率为0.01 mol/(L•m i n) | |
| C. | 升高温度时,逆反应速率大于正反应速率,平衡常数K值会减小 | |
| D. | 平衡时再通入18O2,平衡右移,达新平衡时,18O仅存在于O2和SO3中 |
5.6.4g Cu和足量的硫粉在充分反应,2Cu+S$\frac{\underline{\;\;△\;\;}}{\;}$Cu2S,下列有关叙述正确的是( )
| A. | 反应中氧化剂和还原剂的质量比为1:2 | |
| B. | 反应中生成了8g Cu2S | |
| C. | 反应中有0.2×6.02×1023个电子转移 | |
| D. | 反应中有1.6g硫被氧化 |
15.在水电离出的c(H+)=1×10-14 mol•L-1的溶液中,一定能大量共存的离子组是( )
| A. | K+、Na+、HCO3-、Cl- | B. | K+、AlO2-、Br-、Cl- | ||
| C. | Na+、Cl-、NO3-、SO42- | D. | Al3+、NH4+、Cl-、SO42- |
2.设NA表示阿伏加德罗常数,下列叙述中正确的是( )
| A. | 常温常压下,11.2 LCO2所含的原子数为1.5NA | |
| B. | 标准状况下,22.4 L CCl4中所含分子数为NA | |
| C. | 标准状况下,18g水所含原子数为NA | |
| D. | 常温常压下,48 g O2与O3混合物含有的氧原子数为3NA |
20.下列递变规律不正确的是( )
| A. | Na、Mg、Al还原性依次减弱 | B. | Cl2、Br2、I2氧化性依次增强 | ||
| C. | Be、Mg、Ca与盐酸反应越来越剧烈 | D. | P、S、Cl最高正价依次升高 |
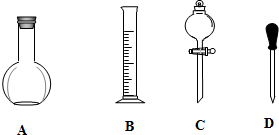 实验室需要0.1mol/LNaOH溶液450mL和0.5mol/L的硫酸溶液500mL.根据这两种溶液的配制情况回答下列问题.
实验室需要0.1mol/LNaOH溶液450mL和0.5mol/L的硫酸溶液500mL.根据这两种溶液的配制情况回答下列问题.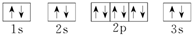 ;D
;D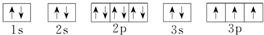 .
.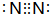 ,氢化物
,氢化物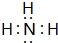 .
.