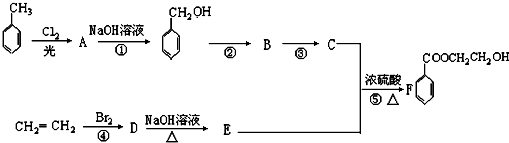
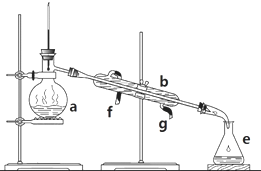
题目内容
A、B、C三元素原子的核外电子数都比氩原子少,A和C处于同主族,且A和C之间不能形成化合物,A元素和B元素的原子两者核电荷数之差为5,B原子核外M层比L电子层少两个电子,则B的原子结构示意图为 ;A离子的结构示意图为 ;A与B形成化合物的化学式是 ,它的电子式是 ,它属于 化合物.(填“离子”或“共价”)C与O2反应的化学方程式为 .
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:A、B、C三元素原子的核外电子数都比氩原子少,B原子核外第3电子层比第2电子层少两个电子,最外层电子数为6,则B为S元素,A元素和B元素的原子两者核电荷数之差为5,故A为Na元素,A和C处于同主族,且A和C之间不能形成化合物,则C为Li元素,据此解答即可.
解答:
解:依据分析可知:A为钠,B为硫,C为锂,
B为S元素,原子结构示意图为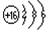 ;A为Na,离子的结构示意图为
;A为Na,离子的结构示意图为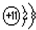 ,Na与S形成化合物的化学式是Na2S,它的电子式是
,Na与S形成化合物的化学式是Na2S,它的电子式是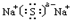 ,它属于离子化合物,锂与氧气反应生成氧化锂,化学反应方程式为:4Li+O2
,它属于离子化合物,锂与氧气反应生成氧化锂,化学反应方程式为:4Li+O2
2Li2O,故答案为: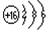 ;
;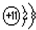 ; Na2S,
; Na2S,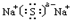 ,离子;4Li+O2
,离子;4Li+O2
2Li2O.
B为S元素,原子结构示意图为
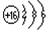 ;A为Na,离子的结构示意图为
;A为Na,离子的结构示意图为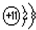 ,Na与S形成化合物的化学式是Na2S,它的电子式是
,Na与S形成化合物的化学式是Na2S,它的电子式是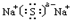 ,它属于离子化合物,锂与氧气反应生成氧化锂,化学反应方程式为:4Li+O2
,它属于离子化合物,锂与氧气反应生成氧化锂,化学反应方程式为:4Li+O2
| ||
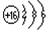 ;
;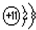 ; Na2S,
; Na2S,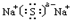 ,离子;4Li+O2
,离子;4Li+O2
| ||
点评:本题主要考查结构与位置关系,比较基础,侧重对化学用语的考查,注意基础知识的掌握.

练习册系列答案
相关题目
对下列物质用途的解释不正确的是( )
| 用途 | 解释 | |
| A | SO2可用于漂白纸浆 | SO2具有氧化性 |
| B | 明矾可用于净水 | 明矾在水中生成的氢氧化铝胶体有吸附性 |
| C | 纯碱可去油污 | 纯碱水解呈碱性 |
| D | “84”消毒液可用于漂白 | 置于空气中生成的次氯酸有氧化性 |
| A、A | B、B | C、C | D、D |
已知25℃时,电离平衡常数Ka(HF)=3.6×10-4 mol/L,溶度积常数Ksp(CaF2)=1.0×10-10 mol3/L3,Ksp(CaCO3)=5×10-9.现向50m L 0.2mol/L HF溶液中加入50mL 0.2mol?L-1 CaCl2溶液,则下列说法中,正确的是( )
| A、25℃时,0.1 mol/L HF溶液pH=1 |
| B、Ksp(CaF2)随温度和浓度的变化而变化 |
| C、向反应后的溶液中继续加入100m L 0.1 mol/L Na2CO3有CaCO3沉淀产生 |
| D、该体系中有CaF2沉淀产生,且反应后溶液中的F-浓度为1×10-4.5mol/L |
对于反应A(g)+3B(g)?2C(g),下列各数据表示不同条件下的反应速率,其中反应进行得最快的是( )
| A、v(A)=0.01 mol/(L?s) |
| B、v(B)=0.04 mol/(L?s) |
| C、v(B)=0.60mol/(L?min) |
| D、v(C)=1.0mol/(L?min) |