题目内容
9.下列有关金属元素的说法正确的是( )| A. | 金属在常温下都是固态 | B. | 金属具有导电性、导热性和延展性 | ||
| C. | 金属都能与稀盐酸反应放出氢气 | D. | 金属在自然界中都是以化合态存在 |
分析 A.金属常温下不全是固体;
B.金属的通性为导电、导热、延展性;
C.不活泼的金属和稀盐酸不能发生反应;
D.自然界中存在游离态的金属金.
解答 解:A.金属在常温下不都是固态,汞为液态,故A错误;
B.金属具有导电性、导热性和延展性,是金属的通性,故B正确;
C.金属活动顺序表中氢元素后边的金属和稀盐酸不发生反应,如铜和稀盐酸不反应,故C错误;
D.金在自然界中都是以游离态存在,故D错误;
故选B.
点评 本题考查了金属的性质分析、金属元素的存在等知识,掌握基础是解题关键,题目难度不大.

练习册系列答案
相关题目
19.下列粒子的核外电子排布正确的是( )
| A. | Na  | B. | K  | C. | Xe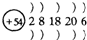 | D. | Cl- |
20.已知A是一种金属单质,B显淡黄色,其转化关系如图所示,则C的以下性质错误的是( )
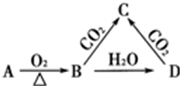

| A. | 与足量盐酸反应放出气体 | B. | 与澄清石灰水反应产生白色沉淀 | ||
| C. | 与氯化钙溶液不反应 | D. | 溶液呈碱性 |
17.已知铋(Bi)元素的化合价可表现为+3或+5价.锗酸铋(简称BGO)是我国研制成功的一种性能优良的闪烁晶体材料,其中的锗(Ge)元素为+4价.BGO可看成由锗和铋两种元素的氧化物所形成的复杂化合物,已知在BGO中两种氧化物所含氧的质量相同,则BGO的化学式可能是( )
| A. | Bi3Ge3O15 | B. | Bi3Ge3O12 | C. | Bi4Ge3O16 | D. | Bi4Ge3O12 |
4.已知反应X+Y═M+N 为放热反应,对该反应的下列说法中正确的( )
| A. | X 的能量一定高于M | |
| B. | Y 的能量一定高于N | |
| C. | X 和Y 的总能量一定高于M 和N 的总能量 | |
| D. | 因该反应为放热反应,故不必加热就可发生 |
14.1g碳与适量水蒸气完全反应生成一氧化碳和氢气,需吸收10.94kJ热量,则下列热化学方程式正确的是( )
| A. | CO(g)+H2(g)═C(s)+H2O(g)△H=-131.28 kJ•mol-1 | |
| B. | C(s)+H2O(g)═CO(g)+H2(g)△H=+10.94 kJ•mol-1 | |
| C. | C(s)+H2O(g)═CO(g)+H2(g)△H=-131.28 kJ•mol-1 | |
| D. | C(s)+H2O(l)═CO(g)+H2(g)△H=+131.28 kJ•mol-1 |
1.用NA表示阿伏加德罗常数,下列叙述正确的是( )
| A. | 标准状况下,22.4L H2O含有的分子数为1NA | |
| B. | 常温常压下,1.06g Na2CO3含有的Na+离子数为0.02NA | |
| C. | 常温常压下,22.4L CO2气体含有原子数为3NA | |
| D. | 物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl-个数为1NA |
18.区分日常生活中的下列各组物质,两种方法都正确的是( )
| 选项 | 需区分的物质 | 实验方法 |
| A | 白酒和白醋 | ①观察颜色②闻气味 |
| B | 食盐和白糖 | ①加稀盐酸②加水溶解 |
| C | 合成纤维和天然纤维 | ①点燃闻气味②观察色泽 |
| D | 酸性厕所清洁剂与碱性厨房清洁剂 | ①测pH②加石灰石 |
| A. | A | B. | B | C. | C | D. | D |