题目内容
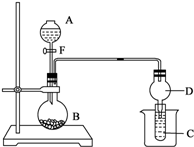 用如图所示装置进行实验,将液体A逐滴加入到固体B中,回答下列问题:
用如图所示装置进行实验,将液体A逐滴加入到固体B中,回答下列问题:(1)图中D装置在实验中的作用是
(2)若A为30%H2O2溶液,B为MnO2,C盛有氢硫酸(H2S)饱和溶液,旋开F后,C中出现浅黄色浑浊的现象,写出C中发生反应的化学方程式为
(3)若A为浓盐酸,B为KMnO4,C中盛有KI淀粉溶液,旋开F后,C中的现象是
(4)若A为浓氨水,B为生石灰,C中盛有AlCl3溶液,旋开F,足够长的时间后,C中的现象是
分析:(1)装置图中D是干燥管上部容积较大,倒吸的液体会靠自身重量回落,起到防止倒吸的作用;
(2)依据反应现象分析,过氧化氢在二氧化锰做催化剂分解生成氧气,氧气会氧化硫化氢生成硫单质;
(3)浓盐酸和高锰酸钾溶液发生氧化还原反应生成氯气,氯气具有强氧化性,和碘化钾反应生成碘单质,遇到淀粉变蓝色;氯气过量会把碘单质氧化为碘酸盐,依据原子守恒和电荷守恒配平书写离子方程式;
(4)AB生成氨气,通入氯化铝溶液中反应生成白色氢氧化铝沉淀和氯化铵.
(2)依据反应现象分析,过氧化氢在二氧化锰做催化剂分解生成氧气,氧气会氧化硫化氢生成硫单质;
(3)浓盐酸和高锰酸钾溶液发生氧化还原反应生成氯气,氯气具有强氧化性,和碘化钾反应生成碘单质,遇到淀粉变蓝色;氯气过量会把碘单质氧化为碘酸盐,依据原子守恒和电荷守恒配平书写离子方程式;
(4)AB生成氨气,通入氯化铝溶液中反应生成白色氢氧化铝沉淀和氯化铵.
解答:解:(1)装置图中D是干燥管上部容积较大,倒吸的液体会靠自身重量回落,起到防止倒吸的作用,
故答案为:防止倒吸;
(2)若A为30%H2O2溶液,B为MnO2,C盛有氢硫酸(H2S)饱和溶液,旋开F后,AB中发生反应,过氧化氢在二氧化锰做催化剂分解生成氧气,C中出现浅黄色浑浊的现象,氧气会氧化硫化氢生成硫单质,C中发生反应的化学方程式为:2H2S+O2═2S↓+2H2O,
故答案为:2H2S+O2═2S↓+2H2O;
(3)若A为浓盐酸,B为KMnO4,C中盛有KI淀粉溶液,旋开F后,AB中发生反应,浓盐酸和高锰酸钾溶液发生氧化还原反应生成氯气,氯气具有强氧化性,和碘化钾反应生成碘单质,遇到淀粉变蓝色,C中的现象是;溶液由无色变为蓝色;氯气过量会把碘单质氧化为碘酸盐,反应的离子方程式为:5Cl2+I2+6H2O═10Cl-+2IO3-+12H+;
故答案为:溶液由无色变为蓝色;5Cl2+I2+6H2O═10Cl-+2IO3-+12H+;
(4)若A为浓氨水,B为生石灰,C中盛有AlCl3溶液,旋开F,AB中浓氨水中溶解氧化钙放热,氨气挥发出来,通入氯化铝溶液中足够长的时间后,反应生成白色氢氧化铝沉淀和氯化铵,氢氧化铝难溶于氨水溶液,C中的现象是产生白色沉淀,反应的离子方程式为:Al3++3NH3?H2O═Al(OH)3↓+3NH4+;
故答案为:产生白色沉淀;Al3++3NH3?H2O═Al(OH)3↓+3NH4+.
故答案为:防止倒吸;
(2)若A为30%H2O2溶液,B为MnO2,C盛有氢硫酸(H2S)饱和溶液,旋开F后,AB中发生反应,过氧化氢在二氧化锰做催化剂分解生成氧气,C中出现浅黄色浑浊的现象,氧气会氧化硫化氢生成硫单质,C中发生反应的化学方程式为:2H2S+O2═2S↓+2H2O,
故答案为:2H2S+O2═2S↓+2H2O;
(3)若A为浓盐酸,B为KMnO4,C中盛有KI淀粉溶液,旋开F后,AB中发生反应,浓盐酸和高锰酸钾溶液发生氧化还原反应生成氯气,氯气具有强氧化性,和碘化钾反应生成碘单质,遇到淀粉变蓝色,C中的现象是;溶液由无色变为蓝色;氯气过量会把碘单质氧化为碘酸盐,反应的离子方程式为:5Cl2+I2+6H2O═10Cl-+2IO3-+12H+;
故答案为:溶液由无色变为蓝色;5Cl2+I2+6H2O═10Cl-+2IO3-+12H+;
(4)若A为浓氨水,B为生石灰,C中盛有AlCl3溶液,旋开F,AB中浓氨水中溶解氧化钙放热,氨气挥发出来,通入氯化铝溶液中足够长的时间后,反应生成白色氢氧化铝沉淀和氯化铵,氢氧化铝难溶于氨水溶液,C中的现象是产生白色沉淀,反应的离子方程式为:Al3++3NH3?H2O═Al(OH)3↓+3NH4+;
故答案为:产生白色沉淀;Al3++3NH3?H2O═Al(OH)3↓+3NH4+.
点评:本题考查了实验探究物质性质的分析应用,主要是物质性质的熟练掌握,题目难度中等.

练习册系列答案
相关题目
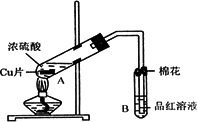
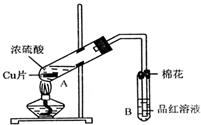
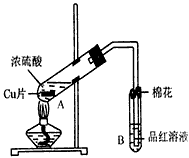
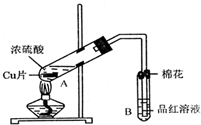 某研究小组用如图所示装置进行铜与浓硫酸反应的实验研究.
某研究小组用如图所示装置进行铜与浓硫酸反应的实验研究.
(1)写出试管B中的实验现象______.
(2)写出A中反应的化学方程式______
(3)继续向A试管中加入H2O2,发现铜片溶解,反应的离子方程式为:______.
若仍不补充浓硫酸,只要求使铜片溶解,也可以加入(填写两种属于不同类别物质的化学式)______、______.
(4)B试管口的棉花应沾有的试剂是______.
(5)小组成员向反应后的溶液中加入足量的氧化铜,使剩余的硫酸全部转化为硫酸铜,过滤后,将滤液加热浓缩,冷却结晶制得硫酸铜晶体(CuSO4?xH2O).小组成员采用加热法测定该晶体里结晶水x的值.
①在他们的实验操作中,至少称量______次;
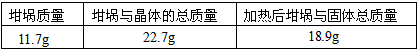
②下面是其中一次实验的数据:
| 坩埚质量 | 坩埚与晶体的总质量 | 加热后坩埚与固体总质量 |
| 11.7g | 22.7g | 18.9g |
A.硫酸铜晶体中含有不挥发的杂质 B.实验前晶体表面有湿存水
C.加热时有晶体飞溅出去 D.加热失水后露置在空气中冷却.
 某研究小组用如图所示装置进行铜与浓硫酸反应的实验研究.
某研究小组用如图所示装置进行铜与浓硫酸反应的实验研究.