题目内容
【题目】下列粒子中,其最外层与最里层的电子数之和等于次外层电子数的是( )
A.S
B.Mg
C.Cl
D.Be
【答案】A
【解析】解:选项中均为短周期元素,由最外层与最内层的电子数之和等于次外层电子数可知,应为3个电子层,最内层的电子数为2,次外层电子数8,最外层电子数,8﹣2=6;
A、S是核外电子排布为:2、8、6,符合题意,故A正确;
B、Mg是核外电子排布为:2、8、2,不符合题意,故B错误;
C、Cl是核外电子排布为:2、8、7,不符合题意,故C错误;
D、Be是核外电子排布为:2、2,不符合题意,故D错误;
故选A.

练习册系列答案
相关题目
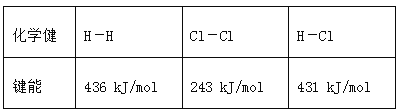
【题目】通常人们把拆开1 mol某化学键所吸收的能量或形成1 mol某化学键所释放的能量看作该化学键的键能,键能的大小可用于估算化学反应的反应热(ΔH),已知
化学健 | H-H | Cl-Cl | H-Cl |
键能 | 436 kJ/mol | 243 kJ/mol | 431 kJ/mol |
化学健 | H-H | Cl-Cl | H-Cl |
键能 | 436 kJ/mol | 243 kJ/mol | 431 kJ/mol |
则下列热化学方程式不正确的是( )
A.![]() H2(g)+
H2(g)+ ![]() Cl2(g)===HCl(g) ΔH=+91.5 kJ·mol-1
Cl2(g)===HCl(g) ΔH=+91.5 kJ·mol-1
B.H2(g)+Cl2(g)===2HCl(g) ΔH=-183 kJ·mol-1
C.2HCl(g)===H2(g)+Cl2(g) ΔH=+183 kJ·mol-1
D.![]() H2(g)+
H2(g)+![]() Cl2(g)===HCl(g) ΔH=-91.5 kJ·mol-1
Cl2(g)===HCl(g) ΔH=-91.5 kJ·mol-1