题目内容
以电解食盐水为基础制取氯气等产品的工业称为“氯碱工业”,它是目前化学工业的重要支柱之一.(1)若电解食盐水时消耗NaCl的质量为234g,则在理论上最多可得氯气的体积为
(2)若将2 mol的氯气通入足量石灰乳中,理论上可得到次氯酸钙
分析:依据电解反应的化学方程式:2NaCl+2H2O
2NaOH+H2↑+Cl2↑来分析计算;
依据化学方程式:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O来分析计算;
| ||
依据化学方程式:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O来分析计算;
解答:解:(1)电解食盐水时消耗NaCl的质量为234g,反应的氯化钠物质的量为
=4mol,
2NaCl+2H2O
2NaOH+H2↑+Cl2↑
4mol 2mol
氯气物质的量为1mol,标准状况下氯气体积为 2mol×22.4L/mol=44.8L,
故答案为:44.8;
(2)2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O;
2mol 1mol
生成次氯酸钙物质的量为1mol,则次氯酸钙质量=1mol×143g/mol=143g,
故答案为:143.
| 234g |
| 58.5g/mol |
2NaCl+2H2O
| ||
4mol 2mol
氯气物质的量为1mol,标准状况下氯气体积为 2mol×22.4L/mol=44.8L,
故答案为:44.8;
(2)2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O;
2mol 1mol
生成次氯酸钙物质的量为1mol,则次氯酸钙质量=1mol×143g/mol=143g,
故答案为:143.
点评:本题考查了化学方程式的计算方法,根据系数之比等于物质的量之比,抓住质量和物质的量的换算计算,气体摩尔体积的换算应用,题目简单.

练习册系列答案
 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目
 海水中可提取多种化工原料,下面是工业上对海水的几项综合利用示意图.
海水中可提取多种化工原料,下面是工业上对海水的几项综合利用示意图.


 MnCl2+Cl2↑+2H2O;根据上述实验原理,从下列装置中选择合适的发生装置用于实验室制取少量氯气
MnCl2+Cl2↑+2H2O;根据上述实验原理,从下列装置中选择合适的发生装置用于实验室制取少量氯气 
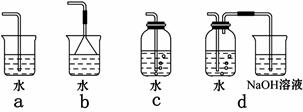

 MnCl2+Cl2↑+2H2O;根据上述实验原理,从下列装置中选择合适的发生装置用于实验室制取少量氯气 (填写装置的序号)。
MnCl2+Cl2↑+2H2O;根据上述实验原理,从下列装置中选择合适的发生装置用于实验室制取少量氯气 (填写装置的序号)。


 MnCl2+Cl2↑+2H2O;根据上述实验原理,从下列装置中选择合适的发生装置用于实验室制取少量氯气
MnCl2+Cl2↑+2H2O;根据上述实验原理,从下列装置中选择合适的发生装置用于实验室制取少量氯气 



