题目内容
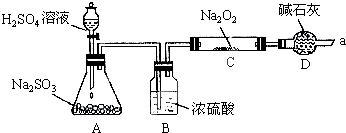
实验室模拟合成氨和氨催化氧化的流程如下:

已知实验室可用饱和亚硝酸钠(NaNO2)溶液与饱和氯化铵溶液经加热后反应制取氮气.
(1)从图中选择制取氮气的合适装置: (填编号)
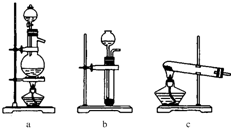
(2)氮气和氢气通过甲装置,甲装置的作用:① ② ③

(3)用乙装置吸收一段时间氨后,再通入空气,同时将经加热的铂丝插入乙装置的锥形瓶内,能说明反应发生的现象是 ,乙装置中的CCl4的作用是 .
(4)反应结束后锥形瓶内的溶液中含有的离子有:H+、OH-、 、 .

已知实验室可用饱和亚硝酸钠(NaNO2)溶液与饱和氯化铵溶液经加热后反应制取氮气.
(1)从图中选择制取氮气的合适装置:

(2)氮气和氢气通过甲装置,甲装置的作用:①

(3)用乙装置吸收一段时间氨后,再通入空气,同时将经加热的铂丝插入乙装置的锥形瓶内,能说明反应发生的现象是
(4)反应结束后锥形瓶内的溶液中含有的离子有:H+、OH-、
考点:工业合成氨,常见气体制备原理及装置选择
专题:氮族元素
分析:(1)实验室可用饱和亚硝酸钠(NaNO2)溶液与饱和氯化铵溶液经加热后反应制取氮气,是溶液与溶液反应,可以选择a;
(2)氮气和氢气通过甲装置,甲装置中的浓硫酸可以将氮气和氢气干燥,同时可以根据甲装置中冒气泡的速率来控制气体流量,混合气体;
(3)根据反应物的性质进行分析,氨的催化氧化生成一氧化氮和水,氨的催化氧化反应为:4NH3+5O2
4NO+6H2O,NO被氧化生成红棕色的NO2,乙装置可以防止倒吸;
(4)氨的催化氧化反应产物是一氧化氮和水,一氧化氮极易与空气中的氧气变为二氧化氮,二氧化氮和水反应生成硝酸和一氧化氮,所以硝酸的存在会和氨水反应生成硝酸铵,溶液中会存在H+、OH-、NH4+、NO3-.
(2)氮气和氢气通过甲装置,甲装置中的浓硫酸可以将氮气和氢气干燥,同时可以根据甲装置中冒气泡的速率来控制气体流量,混合气体;
(3)根据反应物的性质进行分析,氨的催化氧化生成一氧化氮和水,氨的催化氧化反应为:4NH3+5O2
| ||
| △ |
(4)氨的催化氧化反应产物是一氧化氮和水,一氧化氮极易与空气中的氧气变为二氧化氮,二氧化氮和水反应生成硝酸和一氧化氮,所以硝酸的存在会和氨水反应生成硝酸铵,溶液中会存在H+、OH-、NH4+、NO3-.
解答:
解:(1)实验室可用饱和亚硝酸钠(NaNO2)溶液与饱和氯化铵溶液经加热后反应制取氮气,是溶液与溶液反应,可以选择a,故答案为:a;
(2)氮气和氢气通过甲装置,甲装置中的浓硫酸可以将氮气和氢气干燥,同时可以根据甲装置中冒气泡的速率来控制气体流量,混合气体,
故答案为:干燥气体;控制氢气和氮气的流速;混合气体;
(3)根据反应物的性质进行分析,氨的催化氧化生成一氧化氮和水,氨的催化氧化反应为:4NH3+5O2
4NO+6H2O,NO被氧化生成红棕色的NO2,乙装置可以防止倒吸,故答案为:出现红棕色气体;防止倒吸;
(4)氨的催化氧化反应产物是一氧化氮和水,一氧化氮极易与空气中的氧气变为二氧化氮,二氧化氮和水反应生成硝酸和一氧化氮,所以硝酸的存在会和氨水反应生成硝酸铵,溶液中会存在H+、OH-、NH4+、NO3-,故答案为:NH4+;NO3-.
(2)氮气和氢气通过甲装置,甲装置中的浓硫酸可以将氮气和氢气干燥,同时可以根据甲装置中冒气泡的速率来控制气体流量,混合气体,
故答案为:干燥气体;控制氢气和氮气的流速;混合气体;
(3)根据反应物的性质进行分析,氨的催化氧化生成一氧化氮和水,氨的催化氧化反应为:4NH3+5O2
| ||
| △ |
(4)氨的催化氧化反应产物是一氧化氮和水,一氧化氮极易与空气中的氧气变为二氧化氮,二氧化氮和水反应生成硝酸和一氧化氮,所以硝酸的存在会和氨水反应生成硝酸铵,溶液中会存在H+、OH-、NH4+、NO3-,故答案为:NH4+;NO3-.
点评:本题是一道关于氨气的综合题目,解答时需理清相关物质与氨气反应的原理,难度大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列分别是利用不同能源发电的实例图形,其中不属于新能源开发利用的是( )
A、 风力发电 |
B、 太阳能发电 |
C、 火力发电 |
D、 潮汐能发电 |

 得出结论:产物是Na2SO4,该方案是否合理
得出结论:产物是Na2SO4,该方案是否合理