题目内容
5. a、b、c是原子序数依次增大的三种常见短周期元素.由a、b、c三元素组成的化合物甲的用途如下图所示.a、b、c三元素之间两两化合可生成化合物乙、丙、丁、戊4种.化合物甲、乙、丙、丁、戊之间也能相互反应.已知乙、戊分别是由a、b两元素按原子个数1:1和2:1组成的化合物.若a、b、c三元素形成的单质(仍用a、b、c表示)和由它们组成的化合物之间的反应关系如下(未配平)
a、b、c是原子序数依次增大的三种常见短周期元素.由a、b、c三元素组成的化合物甲的用途如下图所示.a、b、c三元素之间两两化合可生成化合物乙、丙、丁、戊4种.化合物甲、乙、丙、丁、戊之间也能相互反应.已知乙、戊分别是由a、b两元素按原子个数1:1和2:1组成的化合物.若a、b、c三元素形成的单质(仍用a、b、c表示)和由它们组成的化合物之间的反应关系如下(未配平)①b+c-→丙 ②a+c-→丁 ③乙+丙-→甲 ④丙+丁-→c+戊
试解答下列问题:
(1)写出下列物质的化学式:
甲:H2SO4,乙:H2O2,丙:SO2,丁:H2S.
(2)写出下列反应的化学方程式:
反应③:H2O2+SO2═H2SO4;
反应④:SO2+2H2S═3S+2H2O.
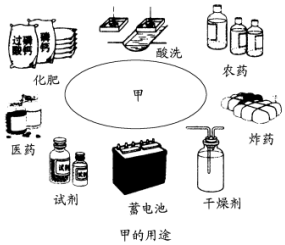
(3)阅读甲的用途图,回答下列问题:
①实验室用甲作干燥剂,这是利用甲的吸水性性质.
②试剂厂用甲和Ca3(PO4)2反应制备化学试剂磷酸,在反应中利用了甲的强酸性性质.
③甲是制造铅蓄电池的重要原料,在铅蓄电池中甲的作用是电解质溶液.
分析 由甲的用途可知甲为H2SO4,则组成元素按原子序数依次增大可知a为H、b为O、c为S元素,乙、戊分别是由a、b两元素按原子个数1:1和2:1组成的化合物,可知乙为H2O2,戊为H2O,乙+丙-→甲,则丙为SO2,a+c-→丁,则丁为H2S,以此解答该题.
解答 解:(1)由以上分析可知甲为H2SO4,乙为H2O2,丙为SO2,丁为H2S,故答案为:H2SO4;H2O2;SO2;H2S;
(2)反应③:为过氧化氢和二氧化硫的反应,方程式为H2O2+SO2═H2SO4,反应④为二氧化硫和硫化氢的反应,方程式为SO2+2H2S═3S+2H2O,
故答案为:H2O2+SO2═H2SO4;SO2+2H2S═3S+2H2O;
(3)①浓硫酸具有吸水性,可用作干燥剂,故答案为:吸水性;
②试剂厂用甲和Ca3(PO4)2反应制备化学试剂磷酸,在反应中利用了甲的强酸性,故答案为:强酸性;
③甲是制造铅蓄电池的重要原料,在铅蓄电池中甲的作用是电解质溶液,故答案为:电解质溶液.
点评 本题考查无机物的推断,为高考常见题型,题目难度中等,注意把握物质的性质、用途,为解答该题的突破口,试题培养了学生灵活应用基础知识的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
16.下列有关0.1mol•L-1 NaOH 溶液的叙述正确的是( )
| A. | 100mL该溶液中含有Na+0.01mol | |
| B. | 1 L该溶液中含有NaOH40 g | |
| C. | 从1L该溶液中取出100mL,所取出的NaOH溶液的浓度为0.01 mol•L-1 | |
| D. | 在1L水中溶解4g NaOH即可配制得0.1 mol•L-1 NaOH溶液 |
13.在下列实验操作与安全事故处理中错误的是( )
| A. | 使用水银温度计测量烧杯中的水浴温度时,不慎打破水银球,用滴管将水银吸出放入水封的小瓶中,残破的温度计插入装有硫粉的广口瓶中 | |
| B. | 用试管夹从试管底部往上夹住距试管口约$\frac{1}{3}$处,手持试管夹长柄末端,进行加热 | |
| C. | 使用滴管取液时,先将滴管伸入试剂瓶中,然后用手指捏紧橡胶乳头,赶出滴管中的空气,放开手指,试剂即被吸入 | |
| D. | 把玻璃导管插入橡胶塞孔时,用厚布护手,紧握用水湿润的插入端,缓慢旋进塞孔中 |
17.用高铁酸钠(Na2FeO4)对河、湖水消毒是城市饮用水处理的新技术,已知反应:Fe2O3+3Na2O2=2Na2FeO4+Na2O.下列说法正确的是( )
| A. | Na2O2既是氧化剂又是还原剂 | |
| B. | Fe2O3在反应中显氧化性 | |
| C. | 1molNa2O2发生反应,有4mol电子转移 | |
| D. | 在Na2FeO4能消毒杀毒是因其具有强氧化性 |
14.在潮湿的空气中,钢铁很快发生电化学腐蚀,在此过程中一定不存在的电极反应是( )
| A. | 2H++2e-=H2↑ | B. | Fe-3e-=Fe3+ | ||
| C. | Fe-2e-=Fe2+ | D. | O2+2H2O+4e-=4OH- |
15.化合物A经李比希法和质谱法分析得知其相对分子质量为136,分子式为C8H8O2.A的核磁共振氢谱有4个峰且面积之比为1:2:2:3,A分子中只含一个苯环且苯环上只有一个取代基,其核磁共振氢谱与红外光谱如图.关于A的下列说法中,正确的是( )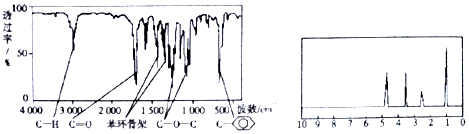

| A. | A分子属于酯类化合物,分子结构中含有酯基和苯基两种官能团 | |
| B. | A在一定条件下可与4 mol H2发生加成反应 | |
| C. | 符合题中A分子结构特征的有机物只有1种 | |
| D. | 与A属于同类化合物的同分异构体只有2种 |
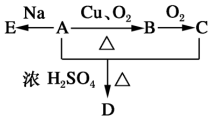 化合物A(C4H10O)是一种有机溶剂,A可以发生如图变化:
化合物A(C4H10O)是一种有机溶剂,A可以发生如图变化: