��Ŀ����
��7�֣���֪Cu��HNO3���Է������·�Ӧ��
Cu + 4HNO3(Ũ)= Cu(NO3)2 + 2NO2��+ 2H2O��3Cu + 8HNO3(ϡ)=3 Cu(NO3)2 + 2NO��+ 4H2O
��֪22.4gͭ��140mLһ��Ũ�ȵ�����ǡ����ȫ��Ӧ��������NO��NO2��������ڱ�״���µ����Ϊ11.2L������
��1����״����NO��NO2������ֱ��Ƕ��٣�
��2��������������ȫ���ͷź�����Һ�м���2mol/L��NaOH��Һ��ǡ��ʹ��Һ�е�Cu2+ȫ��ת��Ϊ����������NaOH��Һ������Ƕ��٣�
���𰸡�
��1��NO��2.24L��2�֣� NO2:8.96L��2�֣� ��2��0.35L����350mL����3�֣�
��������

��ϰ��ϵ�д�
�����Ŀ
 I������ʵ����ơ�������ʵ�������������
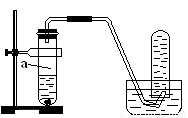
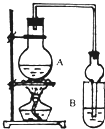
I������ʵ����ơ�������ʵ�������������A������ά�غ������Ϲ��Ⱥ��Һ�壬ȡ���������������Ƶ�Cu��OH��2����Һ���ȣ��۲��Ƿ���ש��ɫ�������ɣ���֤����ά��ˮ������������
B��Һ̬�������м���ϡNaOH��Һ�����ӣ�Ȼ���������ϡHNO3���ټ���AgNO3��Һ����Br-������
C������������Ƿ���м�ȩ��������Ʒ�м�������NaOH��Һ���к�HCOOH������������Ӧʵ��
D�����뱽�ͱ��ӵĻ��Һ����������Ũ��ˮ�����ˣ����ɷ���
E����ͭ˿�ھƾ��������ϼ��Ⱥ�����������ˮ�Ҵ��У�ͭ˿�ָ���ԭ���ĺ�ɫ
F����ȡ�ܽ���ˮ�е������⣺����ƾ��������÷ֲ��ȡ���л����ٷ���
G�����Թ��м���2mL10%��CuSO4��Һ������2%��NaOH��Һ4��6�Σ��������ȩ��Һ0.5mL�����������ڣ�֤����ȩ������
����֪������ˮ�Ȼ��ƿ����Ҵ��γ�������ˮ��CaCl2?6C2H5OH��
���й��л���ķе㣺
| �Լ� | ���� | �Ҵ� | ���� | �������� |
| �е㣨�棩 | 34.7 | 78.5 | 118 | 77.1 |
��1��A��Ũ�����������
��2������ͬλ��18Oʾ�ٷ�ȷ����Ӧ����ˮ��������ԭ�ӵ��ṩ�ߣ�д���ܱ�ʾ18Oλ�õĻ�ѧ��Ӧ����ʽ
��3����ʵ����ʹ�����ιܳ������������⣬��һ��Ҫ������
��4����Ӧ������D�е�������
��5����B�з���������������л�����һ�������Ҵ������Ѻ�ˮ��Ӧ�ȼ�����ˮ�Ȼ��ƣ����˷����
A ���������� B ��ʯ�� C ��ˮ������ D ��ʯ�ң�
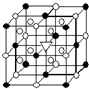 A����1����ͼ��ʾΪ����ʯ����ѧʽΪNa3AlF6���ľ�����ͼ�С�λ�ڴ������嶥������ģ���λ�ڴ��������12������е��8��С����������ģ���ͼ�С��е�һ�֣�ͼ�С�ֱ�ָ����������
A����1����ͼ��ʾΪ����ʯ����ѧʽΪNa3AlF6���ľ�����ͼ�С�λ�ڴ������嶥������ģ���λ�ڴ��������12������е��8��С����������ģ���ͼ�С��е�һ�֣�ͼ�С�ֱ�ָ����������