题目内容
8.下列热化学方程式书写和表示正确的是(△H的绝对值均正确)( )| A. | 2SO2(g)+O2(g)?2SO3(g)△H=-196kJ/mol(反应热) | |
| B. | CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-890.3kJ/mol(燃烧热) | |
| C. | NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)△H=+57.3kJ/mol(中和热) | |
| D. | 2NO2=O2+2NO△H=-116.2kJ/mol(反应热) |
分析 A.二氧化硫和氧气的反应为放热反应;
B.应生成稳定的氧化物,如生成水,应为液态;
C.中和反应为放热反应;
D.NO2的分解为吸热反应,物质的状态没有标出.
解答 解:A.二氧化硫和氧气的反应为放热反应,且标出物质的聚集状态,热化学方程式书写正确,故A正确;
B.表示燃烧热时,应生成稳定的氧化物,甲烷生成水,应为液态,故B错误;
C.中和反应为放热反应,△H<0,故C错误;
D.NO2的分解为吸热反应,△H>0,且应表明物质的聚集状态,故D错误.
故选A.
点评 本题主要考查了热化学方程式书写方法,为高频考点,题目主要是燃烧热、中和热的概念理解和判断,注意热化学方程式书写方法和原则,题目难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
3.下列有关实验的说法不正确的是( )
| A. | 蒸馏时蒸馏烧瓶中液体的体积不能超过容积的$\frac{2}{3}$,液体也不能蒸干 | |
| B. | 可用稀硝酸鉴别MgI2、AgNO3、Na2CO3、NaAlO2四种溶液 | |
| C. | 将Mg(OH)2沉淀转入烧杯中,加足量稀硫酸溶解,加热浓缩、冷却结晶、过滤后得到晶体 | |
| D. | 除去乙酸乙酯中的乙酸杂质:加入氢氧化钠溶液,分液 |
16.取浓度相等的NaOH和HCl溶液,以体积比为3:2的比例相混和,所得溶液中的c(OH-)=0.01mol/L,则原溶液中溶质的物质的量浓度为( )
| A. | 0.01 mol/L | B. | 0.015 mol/L | C. | 0.017 mol/L | D. | 0.05 mol/L |
13.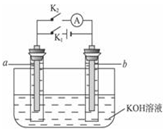 如图所示,a、b是多孔石墨电极,某同学按图装置进行如下实验:断开K2,闭合K1一段时间,观察到两只玻璃管内都有气泡将电极包围,此时断开K1,闭合K2,观察到电流计A的指针有偏转.下列说法不正确的是( )
如图所示,a、b是多孔石墨电极,某同学按图装置进行如下实验:断开K2,闭合K1一段时间,观察到两只玻璃管内都有气泡将电极包围,此时断开K1,闭合K2,观察到电流计A的指针有偏转.下列说法不正确的是( )
 如图所示,a、b是多孔石墨电极,某同学按图装置进行如下实验:断开K2,闭合K1一段时间,观察到两只玻璃管内都有气泡将电极包围,此时断开K1,闭合K2,观察到电流计A的指针有偏转.下列说法不正确的是( )
如图所示,a、b是多孔石墨电极,某同学按图装置进行如下实验:断开K2,闭合K1一段时间,观察到两只玻璃管内都有气泡将电极包围,此时断开K1,闭合K2,观察到电流计A的指针有偏转.下列说法不正确的是( )| A. | 断开K2,闭合K1时,a极上的电极反应式为:4OH--4e-═O2↑+2H2O | |
| B. | 断开K2,闭合K1一段时间,溶液的pH要变大 | |
| C. | 断开K1,闭合K2时,b极上的电极反应式为:2H++2e-═H2↑ | |
| D. | 断开K1,闭合K2时,OH-向b极移动 |
17.化学与社会、技术、环境、生活密切相关.下列有关说法中不正确的是( )
| A. | 高纯度的单晶硅用于制造光导纤维和登月车的光电池 | |
| B. | 石油裂解的主要目的是为了获得短链不饱和烃 | |
| C. | 按照分散质和分散剂所处的状态,可分为9种分散系 | |
| D. | “地沟油”禁止食用,但可以用来制肥皂或生物柴油 |
18.化学在生活中有着广泛的应用,下列对应关系错误的是( )
| 选项 | 性质 | 实际应用 |
| A | SO2具有漂白性 | SO2可用于食品增白 |
| B | SiO2熔点高 | SiO2可用于制作耐高温仪器 |
| C | Al(OH)3具有弱碱性 | Al(OH)3可用于制胃酸中和剂 |
| D | Fe3+具有氧化性 | FeCl3溶液可用于回收废旧电路板中的铜 |
| A. | A | B. | B | C. | C | D. | D |
 ;写出蓝色沉淀溶解在氨水中的离子方程式Cu(OH)2+4NH3•H2O=[Cu(NH3)4]2++2OH-+4H2O.
;写出蓝色沉淀溶解在氨水中的离子方程式Cu(OH)2+4NH3•H2O=[Cu(NH3)4]2++2OH-+4H2O.