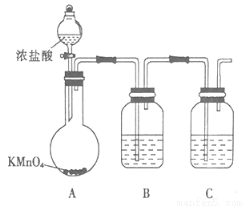
题目内容
下列实验中,对应的现象以及结论都正确的是
选项 | 实验 | 现象 | 结论 |
A | 向酸性KMnO4溶液中滴加H2O2溶液至过量 | 紫色消失 | H2O2在该反应中作还原剂 |
B | 溶有SO2的BaCl2溶液中通入气体X | 有白色沉淀生成 | X一定是Cl2 |
C | 向FeBr2和KSCN混合溶液中滴入少量新制氯水,再加入CCl4混合振荡、静置 | 有机相呈红棕色,水相呈无色 | Fe2+的还原性大于Br- |
D | 铝丝用砂纸打磨后,放在冷的浓硝酸中浸泡一段时间后,放入CuSO4溶液中 | 铝丝表面变红色 | 铝可从铜盐溶液中置换出铜 |
茶叶中含有多种有益于人体健康的有机成分及钙、铁等微量金属元素,某化学研究性学习小组设计方案测定某品牌茶叶中钙元素的质量分数,并检验铁元素的存在(已知CaC2O4为白色沉淀物质).首先取200g茶叶样品焙烧得灰粉后进行如图操作:

请回答下列有关问题:
(1)文献资料显示,某些金属离子的氢氧化物完全沉淀的pH为:
离子 | Ca2+ | Fe3+ |
完全沉淀时的pH | 13 | 4.1 |
实验前要先将茶叶样品高温灼烧成灰粉,其主要目的 。
(2)写出从滤液A→沉淀D的离子反应方程式 。
(3)为保证实验精确度,沉淀D及E需要分别洗涤,并将洗涤液转移回母液中,判断D已经沉淀完全方法是 。
(4)用KMnO4标准溶液滴定C溶液时所发生的反应为:5C2O42-+2MnO4-+16H+═10CO2↑+2Mn2++8H2O。
现将滤液C稀释至500mL,再取其中的25.00mL溶液,用硫酸酸化后,用0.1000mol•L﹣1的KMnO4标准溶液滴定,终点时消耗KMnO4溶液10.00mL.

A B C D
图1 图2
① 此步操作过程中KMnO4标准溶液应装在图2中哪个仪器中(填写字母) 。
②滴定到终点,现象 ,静置后,如图3方法读取KMnO4标准溶液的刻度数据,则测定的钙元素含量将 (填“偏高”“偏低”或“无影响”)。
(5)原茶叶中钙元素的质量分数为 。
化学在生活中有着广泛的应用,下列对应关系错误的是
化学性质 | 实际应用 | |
A. | 三价铁比二价铜氧化性强 | FeCl3腐蚀Cu刻制印刷电路板 |
B. | HF能与Si反应 | 氢氟酸在玻璃器皿上刻蚀标记 |
C. | 次氯酸盐具有氧化性 | 次氯酸钙可做漂白剂 |
D. | 稀硝酸可与银反应 | 稀硝酸可除去试管内壁的银镜 |
1 000mL某待测液中除含有0.2mol,L-1 的Na+外,还可能含有下列离子中的一种或多种:
的Na+外,还可能含有下列离子中的一种或多种:
阳离子 | K+、NH4+、Fe3+、Ba2+ |
阴离子 | Cl-、Br-、CO32-、HCO3-、SO32-、SO42- |
现进行如下实验操作(每次实验所加试剂均过量):

(1)写出生成白色沉淀B的离子方程式:
(2)待测液中 肯定不存在的阳
肯定不存在的阳 离子是 。
离子是 。
(3)若无色气体D是单一气体:
阴离子 | Cl- | Br- | CO32- | HCO3- | SO32- | SO42- |
浓度/mol.L — |
①将阴离子的物质的量浓度填入上表中(一定不存在的填“0”,不能确定的填“? ”):
②判断原溶液中K+是否存在,若存在,求其物质的量浓度的最小值,若不存在,请说明理由:
(4)若无色气体D是混合气体:
①待测液中一定含有的阴离子是 。
② 沉淀A中能与稀硝酸反应的成分是 (写化学式)。
沉淀A中能与稀硝酸反应的成分是 (写化学式)。
| t/s | 0 | t1 | t2 | t3 | t4 |
| n(SO3)/mol | 0 | 0.8 | 1.4 | 1.8 | 1.8 |
| A. | 反应在前t1s的平均速率v(O2)=0.4/t1mol•L-1•s-1 | |
| B. | 保持其他条件不变,体积压缩到1.0L,平衡常数将增大 | |
| C. | 保持温度不变,向该容器中再充入0.3 molSO2、0.1molO2和0.2molSO3,则此时V正>V逆 | |
| D. | 相同温度下,起始时向容器中充入4mol SO3,达到平衡时,SO3的转化率大于10% |


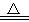 2BCl3+3CO
2BCl3+3CO