��Ŀ����
 I����֪��2SO2��g��+O2��g��?2SO3��g����H=-196.0kJ?mol-1
I����֪��2SO2��g��+O2��g��?2SO3��g����H=-196.0kJ?mol-12NO��g��+O2��g��?2NO2��g����H=-113.0kJ?mol-1
2SO3��l��?2SO3��g����H=20.0kJ?mol-1
��NO2��SO2��Ӧ����SO3��l����һ����ɫ������Ȼ�ѧ����ʽ
����һ�������£���NO2��SO2�������1��2���ں����ܱ������з���������Ӧ��
��������˵����Ӧ�ﵽƽ��״̬����
a����ϵѹǿ���ֲ��� b�����������ɫ���ֲ���
c��SO3��NO�����ʵ���֮�ȱ��ֲ���
d��ÿ����1mol SO3��ͬʱ����1molNO2
�ڸ÷�Ӧ��ƽ��ʱ�����NO2��ת����Ϊ50%����Ӧǰ��������ѹǿ��Ϊ
�ۺ�ѹ�ܱ������з���������Ӧʱ��������Ar����ʹ�÷�Ӧ����
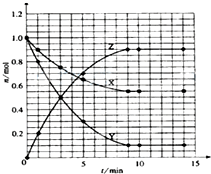
II��ij�¶�ʱ����2L�ܱ���������̬����X��Y��Ӧ������̬����Z�����ǵ����ʵ�����ʱ��ı仯��ͼ��ʾ��������˵����ȷ����
A����Ӧ�Ļ�ѧ����ʽ��X+2Y?2Z
B���÷�Ӧ��0-3minʱ���ڲ���Z��ƽ����Ӧ����0.083mol?L-1?min-1
C���÷�Ӧ�ﵽƽ��ʱ��Ӧ��X��ת���ʦ�����55%
D�������������䣬�����¶ȣ�������Ӧ�����������淴Ӧ���ʽ���С��
���㣺�Ȼ�ѧ����ʽ,��ѧƽ�⽨���Ĺ���,��ѧƽ��״̬���ж�,���ʵ�����Ũ����ʱ��ı仯����
ר�⣺�����������������
�������������Ȼ�ѧ����ʽ��˹���ɼ���õ������Ȼ�ѧ����ʽ��
������ƽ����������ȡ��������ɴ�������һЩ���������жϣ�
�����ݻ�ѧƽ������ʽ��ʽ���㣬����ѹǿ֮�ȵ����������ʵ���֮�ȣ�
�ۺ�ѹ�ܱ������з���������Ӧʱ��������Ar�����������ѹǿ��С��ƽ���������������ķ�����У�
��A������ͼ��XY���ʵ�����С��Z���ʵ�������˵����Ӧ����XY������ΪZ������ͼ����XY��������Z������֮�ȵ��ڻ�ѧ����ʽ������֮�ȼ��������
B�����ݷ�Ӧ����V=
���㷴Ӧ���ʣ�
C��ͼ�������֪ƽ��״̬X������1.0mol-0.55mol=0.45mol�����ת����=
��100%���㣻
D�����ݷ�Ӧ����Ӱ�����ط��������·�Ӧ�����������淴Ӧ���ʶ�����
������ƽ����������ȡ��������ɴ�������һЩ���������жϣ�
�����ݻ�ѧƽ������ʽ��ʽ���㣬����ѹǿ֮�ȵ����������ʵ���֮�ȣ�
�ۺ�ѹ�ܱ������з���������Ӧʱ��������Ar�����������ѹǿ��С��ƽ���������������ķ�����У�
��A������ͼ��XY���ʵ�����С��Z���ʵ�������˵����Ӧ����XY������ΪZ������ͼ����XY��������Z������֮�ȵ��ڻ�ѧ����ʽ������֮�ȼ��������
B�����ݷ�Ӧ����V=
| ��c |
| ��t |
C��ͼ�������֪ƽ��״̬X������1.0mol-0.55mol=0.45mol�����ת����=
| ������ |
| ��ʼ�� |
D�����ݷ�Ӧ����Ӱ�����ط��������·�Ӧ�����������淴Ӧ���ʶ�����
���
�⣺I����2SO2��g��+O2��g��?2SO3��g����H=-196.0kJ?mol-1
��2NO��g��+O2��g��?2NO2��g����H=-113.0kJ?mol-1
��2SO3��l��?2SO3��g����H=20.0kJ?mol-1
���ݸ�˹���ɼ��㣨��-��-�ۣ���
�õ���NO2��g��+SO2��g��?SO3��l��+NO��g����H=-51.5kJ?mol-1��
�ʴ�Ϊ��NO2��g��+SO2��g��?SO3��l��+NO��g����H=-51.5kJ?mol-1��
��a���ɷ�Ӧ��֪������������Һ�壬��Ӧǰ����������ʵ����ı䣬��ϵѹǿʼ�ձ��ֲ��䣬���ж�ƽ��״̬����a��ȷ��
b������������ɫ���ֲ��䣬������������Ũ�Ȳ��䣬�ﵽƽ��״̬����b��ȷ��
c��SO3��NO�ļ�����֮��Ϊ1��1�������Ƿ�ﵽƽ�⣬���ߵ�����ȱ��ֲ��䣬�����ж��Ƿ�ﵽƽ��״̬����c����
d��ÿ����1 mol SO3��ͬʱ����1mol NO2��ֻ���ж�����Ӧ���ʣ�����ȷ�����淴Ӧ���ʵĹ�ϵ�������ж�ƽ��״̬����d����
�ʴ�Ϊ��ab��
�ڽ�NO2��SO2�������1��2���ں����ܱ������з�����Ӧ�������ʵ����ֱ�Ϊx��2x���÷�Ӧ��ƽ��ʱ�����NO2��ת����Ϊ50%��
NO2��g��+SO2��g��?SO3��l��+NO��g��
��ʼ����mol�� x 2x 0 0
�仯����mol�� 0.5x 0.5x 0.5x 0.5x
ƽ������mol�� 0.5x 1.5x 0.5x 0.5x
��Ӧǰ��������ѹǿ��=�������ʵ���֮��=3x����0.5x+1.5x+0.5x��=6��5��
�ʴ�Ϊ��6��5��
�ۺ�ѹ�ܱ������з���������Ӧʱ��������Ar�����������ѹǿ��С��ƽ���������������ķ�����У�ƽ��������У���Ӧ���ʼ�С��
�ʴ�Ϊ����С��
II��A������ͼ��XY���ʵ�����С��Z���ʵ�������˵����Ӧ����XY������ΪZ��ͼ����X����1.0mol-0.55mol=0.45mol��Y������=1.0mol-0.1mol=0.9mol��Z=0.9mol������ͼ����XY��������Z������֮�ȵ��ڻ�ѧ����ʽ������֮��n��X����n��Y����n��Z��=0.45��0.9��0.9=1��2��2����Ӧ�Ļ�ѧ����ʽΪ��X+2Y?2Z����A��ȷ��
B��ͼ�������0-3minZ�����ʵ����仯Ϊ0.5mol�����ݷ�Ӧ����V=
����Z��Ӧ����=
=0.083mol?L-1?min-1����B��ȷ��
C��ͼ�������֪ƽ��״̬X������1.0mol-0.55mol=0.45mol�����ת����=
��100%=
��100%=45%����C����
D�����ݷ�Ӧ����Ӱ�����ط��������·�Ӧ�����������淴Ӧ���ʶ�����D����
�ʴ�Ϊ��AB��
��2NO��g��+O2��g��?2NO2��g����H=-113.0kJ?mol-1
��2SO3��l��?2SO3��g����H=20.0kJ?mol-1
���ݸ�˹���ɼ��㣨��-��-�ۣ���
| 1 |
| 2 |
�ʴ�Ϊ��NO2��g��+SO2��g��?SO3��l��+NO��g����H=-51.5kJ?mol-1��
��a���ɷ�Ӧ��֪������������Һ�壬��Ӧǰ����������ʵ����ı䣬��ϵѹǿʼ�ձ��ֲ��䣬���ж�ƽ��״̬����a��ȷ��
b������������ɫ���ֲ��䣬������������Ũ�Ȳ��䣬�ﵽƽ��״̬����b��ȷ��
c��SO3��NO�ļ�����֮��Ϊ1��1�������Ƿ�ﵽƽ�⣬���ߵ�����ȱ��ֲ��䣬�����ж��Ƿ�ﵽƽ��״̬����c����
d��ÿ����1 mol SO3��ͬʱ����1mol NO2��ֻ���ж�����Ӧ���ʣ�����ȷ�����淴Ӧ���ʵĹ�ϵ�������ж�ƽ��״̬����d����
�ʴ�Ϊ��ab��
�ڽ�NO2��SO2�������1��2���ں����ܱ������з�����Ӧ�������ʵ����ֱ�Ϊx��2x���÷�Ӧ��ƽ��ʱ�����NO2��ת����Ϊ50%��
NO2��g��+SO2��g��?SO3��l��+NO��g��
��ʼ����mol�� x 2x 0 0
�仯����mol�� 0.5x 0.5x 0.5x 0.5x
ƽ������mol�� 0.5x 1.5x 0.5x 0.5x
��Ӧǰ��������ѹǿ��=�������ʵ���֮��=3x����0.5x+1.5x+0.5x��=6��5��
�ʴ�Ϊ��6��5��
�ۺ�ѹ�ܱ������з���������Ӧʱ��������Ar�����������ѹǿ��С��ƽ���������������ķ�����У�ƽ��������У���Ӧ���ʼ�С��
�ʴ�Ϊ����С��
II��A������ͼ��XY���ʵ�����С��Z���ʵ�������˵����Ӧ����XY������ΪZ��ͼ����X����1.0mol-0.55mol=0.45mol��Y������=1.0mol-0.1mol=0.9mol��Z=0.9mol������ͼ����XY��������Z������֮�ȵ��ڻ�ѧ����ʽ������֮��n��X����n��Y����n��Z��=0.45��0.9��0.9=1��2��2����Ӧ�Ļ�ѧ����ʽΪ��X+2Y?2Z����A��ȷ��
B��ͼ�������0-3minZ�����ʵ����仯Ϊ0.5mol�����ݷ�Ӧ����V=
| ��c |
| ��t |
| ||
| 3min |
C��ͼ�������֪ƽ��״̬X������1.0mol-0.55mol=0.45mol�����ת����=
| ������ |
| ��ʼ�� |
| 0.45mol |
| 1.0mol |
D�����ݷ�Ӧ����Ӱ�����ط��������·�Ӧ�����������淴Ӧ���ʶ�����D����
�ʴ�Ϊ��AB��
���������⿼�����Ȼ�ѧ����ʽ��д������˹���ɼ���Ӧ�ã���ѧƽ��Ӱ�����ط������㣬ƽ���־����Ӧ�ã����ջ����ǹؼ�����Ŀ�Ѷ��еȣ�

��ϰ��ϵ�д�
�����Ŀ
