题目内容
(1)同温同压下的两个相同容器中分别装有O2和O3气体,则两瓶气体中分子数之比是 ,原子数之比是 ,质量之比是 ,
(2)下列所给出的几组物质中:含有分子数最多的是 ;含有原子数最多的 是 ;标准状况下体积最大的是 .
①1gH2; ②2.408×1023个CH4; ③10.8gH2O; ④标准状况下6.72LCO2.
(2)下列所给出的几组物质中:含有分子数最多的是
①1gH2; ②2.408×1023个CH4; ③10.8gH2O; ④标准状况下6.72LCO2.
考点:物质的量的相关计算
专题:计算题
分析:同温同压下气体的气体摩尔体积相等,根据n=
=
=
结合分子构成计算.
| V |
| Vm |
| m |
| M |
| N |
| NA |
解答:
解:(1)同温同压下气体的气体摩尔体积相等,由n=
=
=
可知,气体的分子数相等,比值为1:1,则原子数为2:3,质量比等于摩尔质量之比,为2:3,
故答案为:1:1;2:3;2:3;
(2)①n(H2)=
=0.5mol,V(H2)=0.5mol×22.4L/mol=11.2L,原子的物质的量为1mol;
②n(CH4)=
=0.4mol,V(CH4)=0.4mol×22.4L/mol=8.96L,原子的物质的量为2mol;
③n(H2O)=
=0.6mol,原子的物质的量为1.8mol,体积约为10.8mL;
④n(CO2)=
=0.3mol,原子的物质的量为0.9mol,
物质的量越大,分子数越多,最多的是③,原子的物质的量越多,原子个数越多,最多的为②,标准状况下体积最大的是①,
故答案为:③;②;①.
| V |
| Vm |
| m |
| M |
| N |
| NA |
故答案为:1:1;2:3;2:3;
(2)①n(H2)=
| 1g |
| 2g/mol |
②n(CH4)=
| 2.408×1023 |
| 6.02×1023/mol |
③n(H2O)=
| 10.8g |
| 18g/mol |
④n(CO2)=
| 6.72L |
| 22.4L/mol |
物质的量越大,分子数越多,最多的是③,原子的物质的量越多,原子个数越多,最多的为②,标准状况下体积最大的是①,
故答案为:③;②;①.
点评:本题考查物质的量的计算,为高频考点,侧重于学生的分析能力和计算能力的考查,注意把握相关物理量与计算公式的运用,难度不大.

练习册系列答案
 天天练口算系列答案
天天练口算系列答案
相关题目
如图是立方烷的球棍模型,下列有关说法不正确的是( )
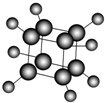

| A、其一氯代物只有一种 |
| B、其二氯代物有三种 |
| C、分子中σ键均由sp3-s电子云重叠而成 |
| D、它与苯乙烯(C6H5-CH=CH2)互为同分异构体 |
下列四个选项是在不同的情况下对化学反应A(g)+3B(g)?2C(g)+2D(g)测得的用不同物质表示的反应速率,其中表示该化学反应的反应速率最快的是( )
| A、v(D)=0.6 mol?L-1?min-1 |
| B、v(A)=0.2 mol?L-1?s-1 |
| C、v(C)=0.40 mol?L-1?min-1 |
| D、v(B)=0.45 mol?L-1?s-1 |