题目内容
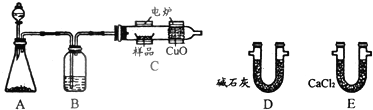
 在有机物分子中,若某个碳原子连接着四个不同的原子或原子团,这种碳原子称为“手性碳原子”.凡有一个手性碳原子的物质一定具有光学活性.如图的物质有光学活性,发生下列反应后生成的有机物无光学活性的是( )
在有机物分子中,若某个碳原子连接着四个不同的原子或原子团,这种碳原子称为“手性碳原子”.凡有一个手性碳原子的物质一定具有光学活性.如图的物质有光学活性,发生下列反应后生成的有机物无光学活性的是( )①与CuO共热
②与NaOH水溶液共热
③与银氨溶液作用
④在催化剂存在下与H2作用
⑤与甲酸发生酯化反应.
| A、全部 | B、①②④⑤ |
| C、①②④ | D、③⑤ |
考点:有机物的结构和性质
专题:有机物的化学性质及推断
分析:某个碳原子连接着四个不同的原子或原子团,这种碳原子称为“手性碳原子”,结合官能团的变化分析碳原子连接的不同基团即可解答.
解答:
解:①与CuO共热,-CH2OH可被氧化生成-CHO,产物含2个-CHO,不具有手性,故选;
②与NaOH水溶液共热,酯基水解生成-CH2OH,产物含2个-CH2OH,不具有手性,故选;
③与银氨溶液作用,-CHO与银氨溶液反应生成-COONH4,仍具有手性碳原子,故不选;
④在催化剂存在下与H2作用,产物含2个-CH2OH,不具有手性,故选;
⑤与甲酸发生酯化反应,与甲酸发生酯化反应,C原子仍连接4个不同的原子或原子团,具有光学活性,故不选.
故选C.
②与NaOH水溶液共热,酯基水解生成-CH2OH,产物含2个-CH2OH,不具有手性,故选;
③与银氨溶液作用,-CHO与银氨溶液反应生成-COONH4,仍具有手性碳原子,故不选;
④在催化剂存在下与H2作用,产物含2个-CH2OH,不具有手性,故选;
⑤与甲酸发生酯化反应,与甲酸发生酯化反应,C原子仍连接4个不同的原子或原子团,具有光学活性,故不选.
故选C.
点评:本题以手性碳考查有机物的结构与性质,注意把握醛、酯、醇的性质是解答的关键,注意体会官能团与性质的关系,题目难度不大.

练习册系列答案
 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案
相关题目
下列反应条件的控制中,不恰当的是( )
| A、为了防止铁生锈,在其表面涂一层防锈油漆 |
| B、为防止火灾,在面粉厂、加油站等场所要严禁烟火 |
| C、为加快KClO3的分解速率,加入MnO2 |
| D、为加快H2O2的分解速率,把反应容器放到冷水中冷却 |
完成如表实验所选择的装置或仪器(夹持装置已略去)正确的是( )
| A | B | C | D | |
| 实验 | 用CCl4提取溴水中的Br2 | 除去乙醇中的苯酚 | 从KI和I2的固体混合物中回收I2 | 配制1000mL0.1000mol?L-1K2Cr2O2溶液 |
| 装置或仪器 |  | 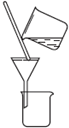 | 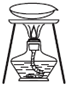 |  |
| A、A | B、B | C、C | D、D |
某兴趣小组为探究外界条件对可逆反应A(g)+B(g)═C(g)+D(s)的影响,进行了如下实验:恒温条件下,往一个容积为10L的密闭容器中充入1mol A和1mol B,反应达平衡时测得容器中各物质的浓度为Ⅰ.然后改变不同条件做了另三组实验,重新达到平衡时容器中各成分的浓度分别为Ⅱ、Ⅲ、Ⅳ.
针对上述系列实验,下列结论中错误的是( )
| A | B | C | |
| Ⅰ | 0.050mol?L-1 | 0.050mol?L-1 | 0.050mol?L-1 |
| Ⅱ | 0.070mol?L-1 | 0.070mol?L-1 | 0.098mol?L-1 |
| Ⅲ | 0.060mol?L-1 | 0.060mol?L-1 | 0.040mol?L-1 |
| Ⅳ | 0.080mol?L-1 | 0.080mol?L-1 | 0.12mol?L-1 |
| A、由Ⅰ中数据可计算出该温度下反应的平衡常数K=20mol-1?L |
| B、Ⅱ可能是通过增大C的浓度实现的 |
| C、若Ⅲ只是升高温度,则与Ⅰ比较,可以判断出正反应一定是放热反应 |
| D、第Ⅳ组实验数据的得出,只能通过压缩容器的体积才可以实现 |
T℃时在2L密闭容器中使X(g)与Y(g)发生反应生成Z(g).反应过程中X、Y、Z的浓度变化如图1所示;若保持其他条件不变,温度分别为T1和T2时,Y的体积百分含量与时间的关系如图2所示.则下列结论不正确的是( )


| A、容器中发生的反应可表示为:3X(g)+Y(g)?2Z(g) |
| B、保持其他条件不变,升高温度,反应的化学平衡常数K增大 |
| C、反应进行的前3min内,用X表示的反应速率v(X)=0.1mol/(L?min) |
| D、若改变反应条件,使反应进程如图3所示,则改变的条件是增大压强 |
下列说法正确的是( )
| A、CH4和Cl2以物质的量之比为1:1混合,光照下只生成CH3Cl和HCl |
| B、分子式为C3H5Cl3的同分异构体共有(不考虑立体异构)5种 |
C、 分子中所有原子可以处在同一平面上 分子中所有原子可以处在同一平面上 |
D、单体CH2═CHCH3和CH2═CH2可以通过加聚反应合成 |
在一定温度下,可逆反应:X(气)+3Y(气)?2Z(气)达到反应限度的是( )
| A、X、Y、Z的浓度相等 |
| B、X、Y、Z的分子数比为1:3:2 |
| C、Z的生成速率是X的生成速率的二倍 |
| D、单位时间内生成n mol X,同时生成3n mol Y |