题目内容
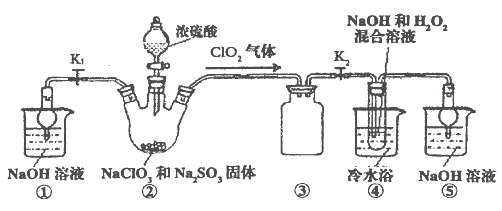
【题目】无水FeCl3在空气中易潮解,遇水水解,加热易升华,实验室可用下列装置制备。
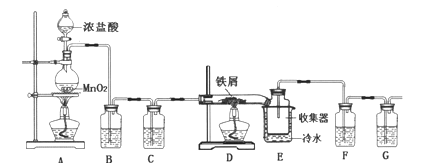
(1)反应开始后,装置D硬质玻璃管中出现的现象为__________。
(2)装置F中所盛的试剂为___________。
(3)下列有关该实验的说法中,不正确的是__________。
A.B装置的作用是除去HCl,并能减少Cl2的溶解
B.E装置中冷水的作用是冷却,使FeCl3冷却沉积
C.若氯气不足则会产生FeCl2
D.向烧瓶中加入足量的AgNO3和稀硝酸,可确定生成的MnCl2的质量
【答案】 出现棕黄色的烟 浓硫酸 CD
【解析】试题分析:装置D中铁与氯气反应只能生成氯化铁,现象是出现棕黄色的烟;(2)无水FeCl3在空气中易潮解,遇水水解,加热易升华,所以在制备装置前后都要连接干燥装置;
解析:(1)装置D硬质玻璃管中生成氯化铁,现象为出现棕黄色的烟;(2)为防止氯化铁遇水水解,装置F中所盛的试剂为浓硫酸;(3)
A.B装置中盛有饱和食盐水的作用是除去HCl,并能减少Cl2的溶解,故A正确;
B. 氯化铁易升华,所以E装置中冷水的作用是冷却,使FeCl3冷却沉积,故B正确;
C.若氯气与铁反应产生FeCl3,故C错误;
D.制取氯气后的溶液中一定有剩余的盐酸,向烧瓶中加入足量的AgNO3和稀硝酸,不能确定生成的MnCl2的质量,故D错误。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目