题目内容
Vml Al2(SO4)3溶液中含有Al3+a g,则SO42-的物质的量浓度为(单位:mol?L-1)( )
A、
| ||
B、
| ||
C、
| ||
D、
|
考点:物质的量浓度
专题:物质的量浓度和溶解度专题
分析:根据n=
计算ag Al3+的物质的量,进而根据c=
计算溶液中Al3+的物质的量浓度,根据化学式可知2c(SO42-)=3c(Al3+),据此计算溶液中SO42-的物质的量浓度.
| m |
| M |
| n |
| V |
解答:
解:agAl3+的物质的量=
=
mol,Al3+的物质的量浓度=
=
mol?L-1,根据化学式可知2c(SO42-)=3c(Al3+),所以溶液中SO42-的物质的量浓度为
mol?L-1×
=
mol?L-1,故选A.
| ag |
| 27g/mol |
| a |
| 27 |
| ||
|
| 1000a |
| 27V |
| 1000a |
| 27V |
| 3 |
| 2 |
| 500a |
| 9V |
点评:本题考查物质的量浓度的有关计算,难度不大,注意理解溶液中电解质离子物质的量浓度之间的关系.

练习册系列答案
相关题目
将10g10%NaOH溶液稀释成50mL,所得稀溶液中NaOH的物质的量浓度为( )
| A、0.02mol?L-1 |
| B、0.05mol?L-1 |
| C、0.25mol?L-1 |
| D、0.5mol?L-1 |
有下列离子的检验及其结论:①向某溶液中加入用盐酸酸化的BaCl2溶液,若产生白色沉淀,说明该溶液中含有SO42-②向某未知溶液中先加入几滴AgNO3溶液,再加入HNO3,若产生白色沉淀,说明未知溶液中含有Cl-③对某无色溶液进行焰色反应,观察到火焰呈黄色,说明该溶液含有Na+,但不能肯定是否含有K+.其中正确的是( )
| A、①②③ | B、①② | C、②③ | D、①③ |
用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A、若5.6 LN2中含有N个氮分子,则阿伏加德罗常数为4N |
| B、1mol?L-1NaCl溶液含有NA个Na+离子 |
| C、14 g CO气体中所含的分子数为0.5NA |
| D、标准状况下,22.4 L CCl4含有的分子总数为NA |
某元素B的核电荷数为Z,已知Bn-和Am+的核外具有相同的电子层结构,则A元素的质子数为( )
| A、Z+n-m |
| B、Z+n+m |
| C、Z-n-m |
| D、Z-n+m |
下列离子方程式中,书写正确的是( )
| A、氢氧化钡溶液和稀硫酸反应:H++SO42-+Ba2++OH-=BaSO4↓+H2O |
| B、碳酸氢钠溶液与氢氧化钠溶液混合:HCO3-+OH-=CO32-+H2O |
| C、氧化亚铁溶于稀盐酸:O2-+2H+=H2O |
| D、稀盐酸滴到石灰石上:CO32-+2H+=CO2↑+H2O |
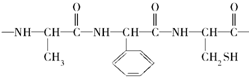 糖类、油脂和蛋白质在人类的生命活动过程中起重要作用,请根据糖类、油脂、蛋白质的有关性质回答下列问题:
糖类、油脂和蛋白质在人类的生命活动过程中起重要作用,请根据糖类、油脂、蛋白质的有关性质回答下列问题:
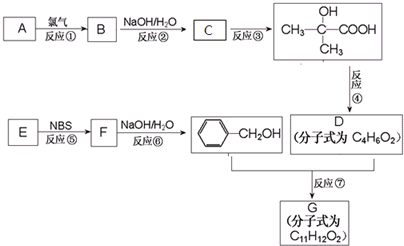
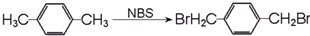
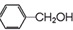 与
与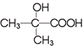 两种有机物,该试剂是
两种有机物,该试剂是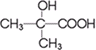 发生缩聚反应生成高分子化合物的结构简式
发生缩聚反应生成高分子化合物的结构简式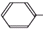 ;C、能使Br2的CCl4溶液褪色.
;C、能使Br2的CCl4溶液褪色.