题目内容
有一硫酸与硝酸的混合溶液,取出10mL加入足量BaCl2溶液,过滤、洗涤、烘干后得到9.32g的沉淀;滤液与4.0mol?L-1NaOH溶液反应,用去35mL碱液时恰好完全中和.试求:
(1)混合液中H2SO4、HNO3的物质的量浓度各是多少?
(2)另取10mL原混合液,加入3.2g铜粉共热时,在标准状况下收集到气体的体积为多少毫升?
(1)混合液中H2SO4、HNO3的物质的量浓度各是多少?
(2)另取10mL原混合液,加入3.2g铜粉共热时,在标准状况下收集到气体的体积为多少毫升?
考点:有关混合物反应的计算
专题:计算题
分析:(1)酸与硝酸的混合溶液,取出10mL加入足量BaCl2溶液,过滤、洗涤、烘干后得到9.32g的沉淀为硫酸钡,根据n=
计算硫酸钡的物质的量,再根据硫酸根守恒n(H2SO4)=n(BaSO4),滤液中氢离子物质的量不变,与4.0mol?L-1NaOH溶液反应,用去35mL碱液时恰好完全中和,酸与氢氧化钠恰好反应,H+与OH-1:1反应,故n(HNO3)+2(H2SO4)=n(NaOH),根据c=
计算硫酸、硝酸的物质的量浓度;
(2)发生3Cu+8H++2NO3-═3Cu2++4H2O+2NO↑,根据反应的离子方程式计算判断反应的过量问题,根据不足量的物质计算生成NO的体积.
| m |
| M |
| n |
| V |
(2)发生3Cu+8H++2NO3-═3Cu2++4H2O+2NO↑,根据反应的离子方程式计算判断反应的过量问题,根据不足量的物质计算生成NO的体积.
解答:
解:(1)硫酸与硝酸的混合溶液,取出10mL加入足量BaCl2溶液,过滤、洗涤、烘干后得到9.32g的沉淀为硫酸钡,
硫酸根守恒,则:n(H2SO4)=n(BaSO4)=
=0.04mol,故原溶液中硫酸浓度为:c(H2SO4)=
=4mol/L;
滤液中氢离子物质的量不变,与4.0mol?L-1NaOH溶液反应,用去35mL碱液时恰好完全中和,酸与氢氧化钠恰好反应中H+与OH-1:1反应,则n(HNO3)+2(H2SO4)=n(NaOH),即:n(HNO3)+2×0.04mol=0.035L×4mol/L,
解得:n(HNO3)=0.06mol,
故原溶液中c(HNO3)=
=6mol/L,
答:混合液中H2SO4、HNO3的物质的量浓度分别为4mol/L、6mol/L;
(2)6.4g铜粉物质的量为:n(Cu)=
=0.05mol,
溶液中氢离子的物质的量为:10×10-3×(4×2+6×1)mol=0.14mol,根据离子方程式:
3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O,
3mol 8mol 44.8L
0.05mol 0.14mol V
0.1mol铜完全反应消耗氢离子的物质的量为:0.05mol×
≈0.133mol,氢离子过量,生成NO的量需要按照铜的物质的量计算,
则生成一氧化氮的体积为:V=
≈0.75L=750mL,
答:在标准状况下收集到气体的体积为750mL.
硫酸根守恒,则:n(H2SO4)=n(BaSO4)=
| 9.32g |
| 233g/mol |
| 0.04mol |
| 0.01L |
滤液中氢离子物质的量不变,与4.0mol?L-1NaOH溶液反应,用去35mL碱液时恰好完全中和,酸与氢氧化钠恰好反应中H+与OH-1:1反应,则n(HNO3)+2(H2SO4)=n(NaOH),即:n(HNO3)+2×0.04mol=0.035L×4mol/L,
解得:n(HNO3)=0.06mol,
故原溶液中c(HNO3)=
| 0.06mol |
| 0.01L |
答:混合液中H2SO4、HNO3的物质的量浓度分别为4mol/L、6mol/L;
(2)6.4g铜粉物质的量为:n(Cu)=
| 3.2g |
| 64g/mol |
溶液中氢离子的物质的量为:10×10-3×(4×2+6×1)mol=0.14mol,根据离子方程式:
3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O,
3mol 8mol 44.8L
0.05mol 0.14mol V
0.1mol铜完全反应消耗氢离子的物质的量为:0.05mol×
| 8 |
| 3 |
则生成一氧化氮的体积为:V=
| 44.8L×0.05mol |
| 3mol |
答:在标准状况下收集到气体的体积为750mL.
点评:本题考查混合物计算、根据方程式进行的计算,题目难度较大,解答关键是明确发生的反应原理,(2)为易错点,注意硫酸和铜不反应,可以提供氢离子,只要氢离子足量,硝酸根就有可能被完全还原.

练习册系列答案
 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案
相关题目
将1mol SO2和1mol O2通入一容积不变的密闭容器中,在一定温度和催化剂作用下,发生反应:2SO2(g)+O2(g)?2SO3(g).反应达到平衡时SO3为0.3mol.若此时移走0.5mol O2和0.5mol SO2,则重新达到平衡后,SO3的物质的量( )
| A、等于0.3 mol |
| B、等于0.15 mol |
| C、小于0.15 mol |
| D、大于0.15 mol,小于0.3 mol |
下列关于油脂的叙述不正确的是( )
| A、属于酯类 |
| B、没有固定的熔沸点 |
| C、是高级脂肪酸的甘油酯 |
| D、油脂的氢化属于氧化反应 |
生活中的一些问题常常涉及到化学知识,下列叙述不正确的是( )
| A、未成熟的苹果遇碘水会变蓝 |
| B、棉花的主要成分是纤维素 |
| C、米饭在嘴中咀嚼有甜味,是因为部分淀粉在唾液淀粉酶催化下发生了水解反应 |
| D、糯米中的淀粉一经水解,就酿成了酒 |
用分液漏斗可以分离的一组物质是( )
| A、苯和醋酸钠溶液 |
| B、苯酚和乙醇 |
| C、乙酸和乙醇 |
| D、植物油和乙酸乙酯 |
反应2A+3B=C+2D在2L的密闭容器中进行,半分钟后,C的物质的量增加了0.3mol,则此反应的平均速率表达正确的是( )
| A、v(C)=0.01 mol?L-1?s-1 |
| B、v(B)=0.03 mol?L-1?s-1 |
| C、v(A)=0.01 mol?L-1?s-1 |
| D、v(D)=0.02 mol?L-1?s-1 |
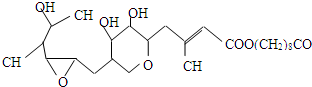
 可以用键线式简单表示为
可以用键线式简单表示为 .则下列与X互为同分异构体的是
.则下列与X互为同分异构体的是
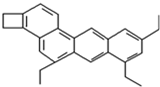
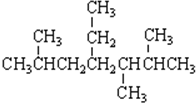 (按系统命名法)名称为
(按系统命名法)名称为