题目内容
(1)如图是目前世界上比较先进的电解饱和食盐水制碱技术--离子交换膜法示意图.
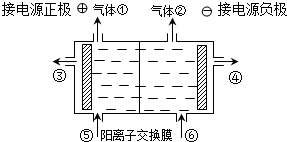
分别写出①、④、⑤各表示什么物质:① ④ ⑤ 该电解反应的离子方程式为
(2)二甲醚(CH3OCH3)直接燃料电池具有启动快、效率高等优点.若电解质为酸性,二甲醚直接燃料电池的正极反应为 ,负极反应为 .

分别写出①、④、⑤各表示什么物质:①
(2)二甲醚(CH3OCH3)直接燃料电池具有启动快、效率高等优点.若电解质为酸性,二甲醚直接燃料电池的正极反应为
考点:电解原理,常见化学电源的种类及其工作原理
专题:电化学专题
分析:(1)左边与电源的正极相连为阳极,发生:2Cl─-2e-=Cl2↑,则右边为阴极,发生2H++2e-=H2↑,电解时,阳极生成氯气,消耗NaCl,则应在阳极(也就是⑤处)补充NaCl,阴极生成OH-,且Na+向阴极移动,则产品烧碱溶液从阴极区(⑥)导出,注意题中阳离子交换膜仅允许Na+通过的特点;
(2)燃料电池中燃料在负极上失电子发生氧化反应,正极发生还原反应,书写电极反应,
(2)燃料电池中燃料在负极上失电子发生氧化反应,正极发生还原反应,书写电极反应,
解答:
解:(1)左边与电源的正极相连为阳极,发生:2Cl─-2e-=Cl2↑,则右边为阴极,发生2H++2e-=H2↑,电解时,阳极生成氯气,消耗NaCl,则应在阳极(也就是⑤处)补充NaCl,阴极生成OH-,且Na+向阴极移动,则产品烧碱溶液从阴极区(⑥)导出,注意题中阳离子交换膜仅允许Na+通过的特点,电解反应的离子方程式为2Cl-+2H2O
H2↑+Cl2↑+2OH-;故答案为:Cl2;氢氧化钠溶液;饱和食盐水;2Cl-+2H2O
H2↑+Cl2↑+2OH-;
(2)若电解质为酸性,氧气在正极发生还原反应,O2+4H++4e-=2H2O,二甲醚直接燃料电池的负极反应为二甲醚失电子生成二氧化碳,结合原子守恒和电荷守恒写出电极反应为:CH3OCH3+3H2O-12e-=2CO2+12H+,故答案为:O2+4H++4e-=2H2O;CH3OCH3+3H2O-12e-=2CO2+12H+.
| ||
| ||
(2)若电解质为酸性,氧气在正极发生还原反应,O2+4H++4e-=2H2O,二甲醚直接燃料电池的负极反应为二甲醚失电子生成二氧化碳,结合原子守恒和电荷守恒写出电极反应为:CH3OCH3+3H2O-12e-=2CO2+12H+,故答案为:O2+4H++4e-=2H2O;CH3OCH3+3H2O-12e-=2CO2+12H+.
点评:本题考查电解原理,侧重于氯碱工业的考查,注意把握题给信息,阳离子交换膜为解答该题的关键,注意审题,题目难度不大.

练习册系列答案
相关题目
金刚石和石墨是碳元素的两种结构不同的单质.在100kPa时,1mol石墨转化为金刚石,要吸收1.895kJ的能量.下列说法不正确的是( )
| A、石墨比金刚石稳定 |
| B、金刚石与石墨中的化学性质相似 |
| C、1mol金刚石比1mol石墨的总能量高 |
| D、1mol石墨和金刚石完全燃烧时释放的能量石墨比金刚石多 |
胶体区别于其他分散系的本质特征是( )
| A、有丁达尔现象 |
| B、有聚沉现象 |
| C、可以无规则的运动 |
| D、分散质粒子直径在1-100nm |
居室装修用石材的放射性常用
Ra作为标准,居里夫人(Marie Curie)因对Ra元素的研究两度获得诺贝尔奖.下列叙述中正确的是( )
226 88 |
| A、Ra元素位于元素周期表中第六周期ⅡA |
| B、RaSO4难溶于水和强酸 |
| C、RaCO3不能与盐酸反应 |
| D、Ra(OH)2是一种两性氢氧化物 |
相对分子质量为100的烃,且含有4个甲基的同分异构体共有(不考虑立体异构)( )
| A、3种 | B、4种 | C、5种 | D、6种 |