题目内容
加热纯碱和小苏打的混合物20g,至质量不再变化时,冷却后称量其固体质量是13.8g,
(1)求原混合物中纯碱和小苏打的质量各是多少?
(2)求原混合物中纯碱的质量分数.
(1)求原混合物中纯碱和小苏打的质量各是多少?
(2)求原混合物中纯碱的质量分数.
考点:有关混合物反应的计算
专题:
分析:加热发生反应:2NaHCO3
Na2CO3+CO2↑+H2O,导致固体质量减少,利用差量法计算碳酸氢钠的质量,进而计算碳酸钠的质量及质量分数.
| ||
解答:
解:设混合物中碳酸氢钠的质量为x,则:
2NaHCO3
Na2CO3+CO2↑+H2O 质量减少
168 62
x 20g-13.8g=6.2g
x=
=16.8g,
所以碳酸钠的质量为20g-16.8g=3.2g,
则原混合物中纯碱的质量分数是
×100%=16%,
答:(1)原混合物中纯碱为3.2g,小苏打的质量是16.8g;
(2)原混合物中纯碱的质量分数为16%.
2NaHCO3
| ||
168 62
x 20g-13.8g=6.2g
x=
| 168×6.2g |
| 62 |
所以碳酸钠的质量为20g-16.8g=3.2g,
则原混合物中纯碱的质量分数是
| 3.2g |
| 20g |
答:(1)原混合物中纯碱为3.2g,小苏打的质量是16.8g;
(2)原混合物中纯碱的质量分数为16%.
点评:本题考查混合物计算,难度不大,侧重于学生的分析能力和计算能力的考查,注意利用差量法进行计算.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列说法正确的是( )
| A、乙烯和苯都能使溴水褪色,退色的原因相同 |
B、用KMnO4酸性溶液鉴别CH3CH═CHCH2OH和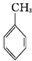 |
| C、乙炔既能使溴水退色,又能使酸性KMnO4溶液退色 |
| D、光照下2,2-二甲基丙烷与Br2反应其一溴取代物有两种 |
下列液体混合物能用分液漏斗分离的是( )
| A、苯和甲苯 | B、乙醇和水 |
| C、溴乙烷和苯 | D、溴乙烷和水 |
下列说法或表示方法中正确的是( )
| A、等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多 |
| B、由C(金刚石)→C(石墨)△H=-1.9KJ/mol 可知,金刚石比石墨稳定 |
| C、在101KPa时,2gH2完全燃烧生成液态水,放出285.8KJ热量,氢气燃烧的热化学方程式为:2H2(g)+O2(g)=2H2O(l)△H=+285.8KJ/mol |
| D、向纯水中加入硫酸氢钠,水的电离程度减小,Kw值不变 |