题目内容
3.实验室以铜、稀硫酸、硝酸为原料制取硫酸铜晶体的原理如下:将适量硝酸分多次加入到铜粉与稀硫酸的混合物中,加热使之反应完全,通过蒸发、结晶得到硫酸铜晶体.请回答下列问题:
(1)为了节约原料,硫酸和硝酸的物质的量之比最佳为:3:2.
(2)为了吸收该反应中产生的尾气,请选择下列装置中合适的装置序号B.
(3)为了使制备实验更加符合绿色化学的要求,某校化学研究性学习小组进行如下设计:
第一组:以空气为氧化剂法.
【方案1】将铜粉在坩埚(填仪器名称)中反复灼烧,使铜与空气充分反应生成氧化铜,再将氧化铜与稀硫酸反应.
【方案2】将空气直接通入到铜粉与稀硫酸的混合物中,发现在常温下几乎不反应.向反应液中加少量FeSO4,即发生反应,生成硫酸铜.反应完全后,加物质甲调节pH,铁元素全部沉淀(注:铁离子的浓度下降到10-5mol•L-1,就认为沉淀完全),然后过滤、浓缩、结晶.
已知:Ksp[Cu((OH)2]≈10-22,Ksp[Fe((OH)2]≈10-16,Ksp[Fe((OH)3]≈10-38若开始时加入的铜粉为3.2g,最后所得溶液为500mL,溶液中含有铁元素0.005mol.则:
①为了使铁元素全部沉淀,应调节pH至少为3.
②上述物质甲不可以选用的物质是BE.
A、CuO B、NaOH C、CuCO3 D、Cu2(OH)2CO3 E、Fe2(SO4)3 F、Cu(OH)2
③反应中加入少量FeSO4可加速铜的氧化,用离子方程式解释其原因如下:4Fe2++O2+4H+═4Fe3++2H2O、2Fe3++Cu═2Fe2++Cu2+.
第二组:以过氧化氢为氧化剂法.
将3.2g铜丝放到45mL 1.5mol•L-1的稀硫酸中,控温在50℃,再加入18mL 10%的H2O2,反应0.5h;然后升温至60℃,持续反应1h.反应后先过滤除去过量的铜;再蒸发浓缩、冷却结晶、过滤并用少量95%的酒精淋洗后晾干,称量得CuSO4•5H2O 10.5g.则:
④反应时温度控制在50℃~60℃不宜过高的原因是防止双氧水分解.
⑤本实验中CuSO4•5H2O的产率为84%.
分析 (1)依据铜和稀硝酸反应的离子方程式,理解反应实质氢离子是硫酸和硝酸提供;尾气只要是一氧化氮、二氧化氮,需要和氧气混合通入碱溶液中完全吸收;
(2)固体灼烧应在坩埚内;
①依据Ksp和一般认为铁离子的浓度下降到10-5mol•L-1,就认为沉淀完全,计算溶液PH;
②调节溶液PH和溶液中氢离子反应,提高溶液PH,但不能引入新的杂质;
③亚铁离子在空气中易被氧化为铁离子,铜能溶解于含铁离子的溶液中;
④根据双氧水加热易分解的性质分析;
⑤依据固体条件结合得到硫酸铜晶体质量计算得到.
解答 解:(1)验室用铜制取硫酸铜,将适量硝酸分多次加入到铜粉与稀硫酸的混合物中,加热使之反应完全,反应的离子方程式为:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O,依据离子反应实质,氢离子是硝酸和硫酸共同提供,氢离子分析可知最佳比为6:2,所以硫酸和硝酸物质的量之比最佳为3:2;吸收该反应中产生的尾气氮的氧化物需要通入氧气混合后通入氢氧化钠溶液被完全吸收;
A、一氧化氮不能被氢氧化钠吸收,故A错误;
B、空气和一氧化氮通入氢氧化钠溶液可以被吸收,故B正确;
C、空气未通入氢氧化钠溶液,一氧化氮不能在溶液中和氧气反应被氢氧化钠吸收,故C错误;
D、气体都未通入氢氧化钠溶液中,不能被吸收,故D错误;
故答案为:3:2;B;
(2)固体在空气中灼烧需要高温应在坩埚内完成,故答案为:坩埚;
①Ksp[Fe((OH)3]≈10-38 ,依据沉淀溶解平衡可知,c(Fe3+)×c3(OH-)=10-38,一般认为铁离子的浓度下降到10-5mol•L-1,
c(OH-)=10-11mol/L,c(H+)=10-3mol/L,pH=3,故答案为:3;
②除杂的原则,保证不引入杂质,加入氧化铜或碱式碳酸铜都能能和酸反应提高溶液PH,但不引进新的杂质,加入CaO、NaOH、Fe2(SO4)3会引入新的杂质离子,得不到纯净的硫酸铜晶体,故答案为:CD;
③反应中加入少量FeSO4可加速铜的氧化,亚铁离子酸性溶液中被空气中的氧气氧化为铁离子,铁离子溶解铜生成硫酸铁和硫酸铜,反应的两种方程式为:4Fe2++O2+4H+═4Fe3++2H2O; 2Fe3++Cu═2Fe2++Cu2+,故答案为:4Fe2++O2+4H+═4Fe3++2H2O,2Fe3++Cu═2Fe2++Cu2+;
④过氧化氢不稳定,温度过高易分解生成水和氧气,故答案为:防止双氧水分解;
⑤设3.2g铜生成五水硫酸铜的质量为xg,根据铜原子守恒得铜和五水硫酸铜的关系式为:
Cu→CuSO4•5H2O
64g 250g
3.2g xg
所以x=12.5g
理论上生成CuSO4•5H2O 12.5克,故产率为$\frac{10.6g}{12.5g}$×100%=84.8%,
故答案为:84.8%.
点评 本题考查了制备物质的实验设计和方案探究,实验装置的应用分析,物质性质的判断,氧化还原反应的分析,尾气处理方法,溶液PH的计算,制备物质产率计算,题目综合性强,需要扎实的基础知识,题目难度中等.

| A. | HX | B. | H2X | C. | XH3 | D. | XH4 |
| A. | 100 mL | B. | 500 mL | C. | 1000 mL | D. | 1500 mL |
| A. | 可用丁达尔现象区分溶液与胶体 | |
| B. | 生石灰与水混合的过程只发生物理变化 | |
| C. | O3是由3个氧原子构成的化合物 | |
| D. | CuSO4•5H2O是一种混合物 |

已知:在水浸后的Na2CrO4溶液中含有少量NaAlO2、Na2ZnO2等物质.
(1)水浸后的溶液呈碱性(填“酸”、“碱”或“中”).
(2)完成氧化焙烧过程中生成Na2CrO4的化学方程式.
4Cr(OH)3+4Na2CO3+3O2$\frac{\underline{\;中温\;}}{\;}$4Na2CrO4+4CO2+6H2O
(3)滤渣Ⅱ的主要成分有Zn(OH)2、Al(OH)3.
已知:①除去滤渣II后,溶液中存在如下反应:2Cr+2H+?Cr2+H2O
②Na2Cr2O7、Na2CrO4在不同温度下的溶解度如下表
温度 溶解度 化学式 | 20℃ | 60℃ | 100℃ |
| Na2SO4 | 19.5 | 45.3 | 42.5 |
| Na2Cr2O7 | 183 | 269 | 415 |
| Na2CrO4 | 84 | 115 | 126 |
(5)工业上还可以在水浸过滤后的溶液(Na2CrO4)加入适量H2SO4,用石墨作电极电解生产金属铬,写出生成铬的电极反应方程式CrO42-+8H++6e-=Cr+4H2O.
(6)已知Al(OH)3为难溶物(常温下,Ksp[Al(OH)3]=2.0×10-33).当溶液pH=5时,某溶液中的Al3+能(填“能”或“不能”)完全沉淀.(溶液中的离子浓度小于1×10-5 mol•L-1时沉淀完全).
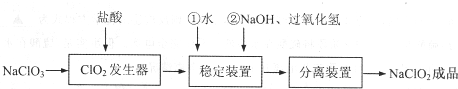
已知NaClO2的溶解度随温度升高而增大,适当条件下可结晶析出NaClO2•3H2O且NaClO2在碱性条件下稳定性较高.试回答下列问题:
(1)在ClO2发生器中同时有氯气产生,则在发生器中发生反应的化学方程式为2NaClO3+4HCl=2NaCl+2ClO2↑+Cl2↑+2H2O.
(2)在稳定装置中生成NaClO2,H2O2作B(选填序号).
A.氧化剂 B.还原剂 C.既作氧化剂又作还原剂 D.既不作氧化剂也不作还原剂
反应生成NaClO2的化学方程式为2NaOH+2ClO2+H2O2=2NaClO2+2H2O+O2.
(3)在实验室模拟“固体分离装置”中的技术(即从溶液中分离出溶质),必须进行的实验操作是BEA(按实验先后顺序填写操作代号).
A.过滤 B.加热 C.分液 D.蒸馏 E.冷却 F.萃取
(4)经查阅资料知道:①当pH≤2.0时,ClO2-能被I-完全还原成Cl-;
②溶液中能发生反应:2S2O32-+I2=2I-+S4O62-.
欲测定成品中NaClO2的含量,现进行如下操作:
| 步骤Ⅰ | 称取NaClO2样品Wg,加水配成溶液置于锥形瓶中,并调节pH≤2.0 |
| 步骤Ⅱ | 向锥形瓶中加入足量KI晶体,充分搅拌,并加入少量指示剂 |
| 步骤Ⅲ | 用c mol•L-1的 Na2S2O3溶液滴定 |
②步骤Ⅲ中达到滴定终点时的现象是滴入最后一滴标准溶液,溶液由蓝色变化为无色且半分钟不变化.
若上述滴定操作中用去了V mL Na2S2O3溶液,则样品中NaClO2的质量分数$\frac{9.05×10{\;}^{-2}VC}{4W}$(用有关字母表示).
(5)ClO2是新型饮用水消毒剂,Cl2常用于饮用水消毒.等物质的量的物质,ClO2的消毒效率是Cl2的2.5倍.
| A. | 除去苯中混有的苯酚可加入浓溴水后过滤 | |
| B. | 向淀粉溶液中滴加稀硫酸后,加热,再加入新制Cu(OH)2加热,没有出现红色沉淀,说明淀粉没有发生水解反应 | |
| C. | 向NaOH溶液中加入溴乙烷,加热,再加入AgNO3溶液,产生沉淀,说明溴乙烷发生了水解反应 | |
| D. | 向酸性KMnO4溶液中滴加维生素C溶液,KMnO4溶液褪色,说明维生素C有还原性 |
| A. | HCl  | B. | NaCl  | C. | HClO H-Cl-O | D. | CO2 O=C=O |
