题目内容
某无色透明溶液能与铝作用放出氢气,且溶液中的离子能大量共存的是( )
| A、K+、NO3-、H+、Cl- |
| B、Cu2+、SO42-、H+、Na+ |
| C、Na+、Ba2+、OH-、NO3- |
| D、NH4+、OH-、Cl-、K+ |
考点:离子共存问题
专题:离子反应专题
分析:无色透明溶液中不存在有色的离子,能与铝作用放出氢气的溶液为酸性或者碱性溶液,
A.硝酸根离子在酸性条件下具有强氧化性,无法与铝反应生成氢气;
B.铜离子为 有色离子,不满足溶液无色的条件;
C.Na+、Ba2+、OH-、NO3-之间不发生反应,且为无色溶液,能够与铝反应生成氢气;
D.铵根离子与氢氧根离子反应生成弱电解质一水合氨.
A.硝酸根离子在酸性条件下具有强氧化性,无法与铝反应生成氢气;
B.铜离子为 有色离子,不满足溶液无色的条件;
C.Na+、Ba2+、OH-、NO3-之间不发生反应,且为无色溶液,能够与铝反应生成氢气;
D.铵根离子与氢氧根离子反应生成弱电解质一水合氨.
解答:
解:该溶液中不存在有色离子,如Cu2+、Fe2+、Fe3+、MnO4-等;与铝反应生成氢气,更溶液中存在大量氢离子或者氢氧根离子,
A.NO3-在H+存在条件下具有氧化性,不能与铝反应生成氢气,故A错误;
B.Cu2+为有色的离子,不满足溶液无色的要求,故B错误;
C.Na+、Ba2+、OH-、NO3-之间不发生反应,能够与铝反应生成氢气,且都是无色离子,在溶液中能够大量共存,故C正确;
D.NH4+、OH-之间能够发生反应生成一水合氨,在溶液中不能大量共存,故D错误;
A.NO3-在H+存在条件下具有氧化性,不能与铝反应生成氢气,故A错误;
B.Cu2+为有色的离子,不满足溶液无色的要求,故B错误;
C.Na+、Ba2+、OH-、NO3-之间不发生反应,能够与铝反应生成氢气,且都是无色离子,在溶液中能够大量共存,故C正确;
D.NH4+、OH-之间能够发生反应生成一水合氨,在溶液中不能大量共存,故D错误;
点评:本题考查离子共存的正误判断,题目难度中等,注意掌握离子反应发生条件,明确离子不能大量共存的一般情况,如:能发生复分解反应的离子之间;能生成难溶物的离子之间;能发生氧化还原反应的离子之间等;解决离子共存问题时还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的颜色,如无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
用固体NaOH配制物质的量浓度溶液时,下列操作会导致溶液浓度偏高的是( )
| A、在烧杯中溶解时,有少量液体溅出 |
| B、样品中含有少量Na2O杂质 |
| C、容量瓶使用前未干燥 |
| D、定容时仰视视容量瓶刻度线 |
下列各项中,正确的是( )
A、Na的原子结构示意图: | ||
| B、N2分子的结构式:N=N | ||
C、HCl的电子式: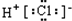 | ||
D、中子数为1的氢原子符号:
|
下列分子的电子式书写正确的是( )
A、氨气  |
B、四氯化碳  |
C、氮气  |
D、二氧化碳  |
下列事实不可以用勒夏特列原理解释的是( )
| A、工业生产硫酸的过程中使用过量氧气,以提高SO2的转化率 |
| B、使用铁触媒作催化剂,加快N2和H2的混合气体合成氨气的速率 |
| C、Fe(SCN)3溶液(Fe3++3SCN-?Fe(SCN)3)中加入固体KSCN后颜色变深 |
| D、开启啤酒瓶后,瓶中马上泛起大量泡沫 |
 北京奥运会期间对大量盆栽鲜花施用了S-诱抗素制剂,以保证鲜花盛开,S-诱抗素的分子结构如图,下列关于该分子说法正确的是( )
北京奥运会期间对大量盆栽鲜花施用了S-诱抗素制剂,以保证鲜花盛开,S-诱抗素的分子结构如图,下列关于该分子说法正确的是( )| A、分子式为C15H22O3 |
| B、1mol该物质最多可以消耗H2和Br2的量都是3mol |
| C、含有碳碳双键、羟基、羰基、羧基 |
| D、该物质不能发生缩聚反应和加聚反应 |
能源与人类的生活和社会发展密切相关.下列关于能源开发和利用的说法不正确的是( )
| A、人类利用的能源都是通过化学反应获得的 |
| B、煤、石油、天然气是不可再生能源 |
| C、在农村提倡利用沼气作生活燃料 |
| D、未来可用乙醇代替汽油作汽车燃料 |
下列化工方法不属于化学变化的是( )
| A、分馏 | B、裂化 | C、裂解 | D、干馏 |
下列叙述正确的是( )
| A、ⅠA族元素单质的熔点从上往下逐渐降低 |
| B、分子晶体中一定存在共价键 |
| C、ⅥA族元素的氢化物中,稳定性最好的其沸点也最高 |
| D、同周期非金属氧化物对应的水化物的酸性从左往右依次增强 |