题目内容
当光束通过下列每组分散系时,不能通过观察丁达尔效应进行区分的是( )
| A、H2SiO3胶体和NaCl溶液 |
| B、FeCl3溶液和Fe(OH)3胶体 |
| C、豆浆和蔗糖溶液 |
| D、CuSO4溶液和Na2SO4溶液 |
考点:分散系、胶体与溶液的概念及关系
专题:溶液和胶体专题
分析:胶体具有丁达尔现象是指当光束通过胶体分散系时能看到一条光亮的通路,丁达尔现象是区分胶体和溶液最常用的简单方法.
解答:
解:A.H2SiO3胶体属于胶体分散系,用光束照射能观察到丁达尔现象,NaCl溶液是溶液无丁达尔效应,故A正确;
B.Fe(OH)3胶体属于胶体分散系,用光束照射能观察到丁达尔现象,FeCl3溶液是溶液无丁达尔效应,故B正确;
C.豆浆属于胶体分散系,用光束照射能观察到丁达尔现象,蔗糖溶液是溶液无丁达尔效应,故C正确;
D.CuSO4溶液和Na2SO4溶液都是溶液,都无丁达尔效应,故D错误.
故选D.
B.Fe(OH)3胶体属于胶体分散系,用光束照射能观察到丁达尔现象,FeCl3溶液是溶液无丁达尔效应,故B正确;
C.豆浆属于胶体分散系,用光束照射能观察到丁达尔现象,蔗糖溶液是溶液无丁达尔效应,故C正确;
D.CuSO4溶液和Na2SO4溶液都是溶液,都无丁达尔效应,故D错误.
故选D.
点评:本题考查胶体的性质,注意胶体的本质特征是:胶体粒子的微粒直径在1-100nm之间,这也是胶体与其它分散系的本质区别,区分胶体和溶液最简单的方法是利用丁达尔现象.

练习册系列答案
相关题目
下列电解质溶液中,离子浓度关系正确的是( )
| A、(NH4)2Fe(SO4)2溶液中:c(SO42-)>c(Fe2+)>c(NH4+)>c(H+)>c(OH-) |
| B、PH相等的①CH3COONa②NaAlO2溶液比较:c(Na+):①<② |
| C、NH4HSO4溶液中:c(H+)>c(OH-)+c(SO42-) |
| D、NaAlO2溶液中通入过量CO2后:c(Na+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+) |
同温同压,相同体积的CO和C2H4具有相同的( )
①分子数 ②原子总数 ③碳原子数 ④质量.
①分子数 ②原子总数 ③碳原子数 ④质量.
| A、①②③④ |
| B、②③④ |
| C、①④ |
| D、①②③ 点燃 |
A、B、C、D、E是原子序数依次增大的五种短周期元素.B和D同主族,可组成共价化合物DB2,B和C最外层电子数之和与E的最外层电子数相同,25℃时0.01mol?L-1A和E形成化合物的水溶液pH为2.下列说法正确的是( )
| A、由于非金属性B>D,则A、B组成化合物的沸点高于A、D组成的化合物 |
| B、在C、B形成的两种离子化合物中阴阳离子的个数比分别为1:2和1:1 |
| C、原子半径由大到小排列的是:C>D>E>B>A |
| D、B、C、E三种元素组成化合物的水溶液一定显碱性 |
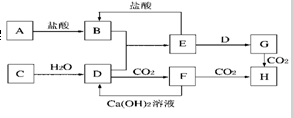
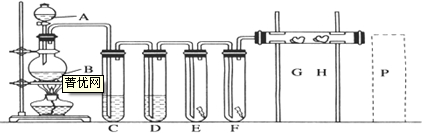

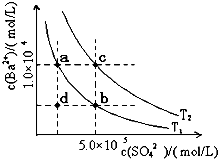 回答下列问题:
回答下列问题: