��Ŀ����
ˮ����������������������Ӧ�ù㷺���Թ�ҵ��ˮ��������ˮ���д����Ƿ�ֹˮ����Ⱦ������ˮ�ʵ���Ҫ��ʩ��
��1��ˮ�ľ����������������� ��
��2����������ˮ���뱣֤��ȫ������ˮ����Ҫ��ȡ�Խ��Ӻ����еĵ�ˮ����ɱ���������������������˵ȹ��մ����������������ȷ˳���� ��
�������Լ��ܹ�����������ˮ����ɱ���������Ҳ�����ɶ�����Ⱦ���� ����ĸ����
a���������� b��Ư�� c������ d������
��3��Na2FeO4��һ������ˮ����������ҵ�Ͽ���FeSO4�Ʊ�Na2FeO4�乤���������£�

�ٹ�ҵ�ϳ���������������������ȥ��Ȼˮ�к��е�������ͽ��壬Ϊ�˴ﵽ���õ�Ч����Ҫ��������ˮ��pH����9���ң��ټ����̷����������һ������ԭ�� �����ñ�Ҫ�����ӷ���ʽ��������������
��д����Fe��0H��3��ȡNa2FeO4�Ļ�ѧ����ʽ�� ��
��4��ʯ�Ҵ���dz��õ�Ӳˮ������������֪25��ʱKsp��CaCO3��=2.8��10-9���ֽ��������Ca��OH��2��Һ��Na2CO3��Һ��ϣ�������Һ������мӺ��ԣ�����Na2CO3��Һ��Ũ��Ϊ5.6��10-5mol?L-1�������ɳ�������Ca��0H��2��Һ����СŨ��Ϊ ��
��1��ˮ�ľ�����������������
��2����������ˮ���뱣֤��ȫ������ˮ����Ҫ��ȡ�Խ��Ӻ����еĵ�ˮ����ɱ���������������������˵ȹ��մ����������������ȷ˳����
�������Լ��ܹ�����������ˮ����ɱ���������Ҳ�����ɶ�����Ⱦ����
a���������� b��Ư�� c������ d������
��3��Na2FeO4��һ������ˮ����������ҵ�Ͽ���FeSO4�Ʊ�Na2FeO4�乤���������£�

�ٹ�ҵ�ϳ���������������������ȥ��Ȼˮ�к��е�������ͽ��壬Ϊ�˴ﵽ���õ�Ч����Ҫ��������ˮ��pH����9���ң��ټ����̷����������һ������ԭ��
��д����Fe��0H��3��ȡNa2FeO4�Ļ�ѧ����ʽ��
��4��ʯ�Ҵ���dz��õ�Ӳˮ������������֪25��ʱKsp��CaCO3��=2.8��10-9���ֽ��������Ca��OH��2��Һ��Na2CO3��Һ��ϣ�������Һ������мӺ��ԣ�����Na2CO3��Һ��Ũ��Ϊ5.6��10-5mol?L-1�������ɳ�������Ca��0H��2��Һ����СŨ��Ϊ
���㣺���ʷ��롢�ᴿ��ʵ�鷽�����
ר�⣺ʵ�������
��������1��������ȥ�������ʣ�������ȥˮ�иơ�þ���ӣ�
��2�����ȳ������ٹ��ˣ��������������
�ڶ�����ˮ����ɱ���������Ҳ�����ɶ�����Ⱦ��ֻ�г����Ļ�ԭ�����ˮ����Ⱦ��
��3���ٽ�������ˮ��pH����9���ң��ټ����̷����ɵõ������ӣ�ˮ�����ɽ��壻
�ڷ���������ԭ��Ӧ����Na2FeO4��
��4��Na2CO3��Һ��Ũ��Ϊ2.8��10-5mol/L���������Ϻ���Һ��c��CO32-��=1.4��10-5mol/L������Ksp=c��CO32-��?c��Ca2+���������ʱ�����Һ��c��Ca2+�����Դ������
��2�����ȳ������ٹ��ˣ��������������
�ڶ�����ˮ����ɱ���������Ҳ�����ɶ�����Ⱦ��ֻ�г����Ļ�ԭ�����ˮ����Ⱦ��
��3���ٽ�������ˮ��pH����9���ң��ټ����̷����ɵõ������ӣ�ˮ�����ɽ��壻
�ڷ���������ԭ��Ӧ����Na2FeO4��
��4��Na2CO3��Һ��Ũ��Ϊ2.8��10-5mol/L���������Ϻ���Һ��c��CO32-��=1.4��10-5mol/L������Ksp=c��CO32-��?c��Ca2+���������ʱ�����Һ��c��Ca2+�����Դ������
���
�⣺��1��ˮ�ľ�����������������ˮ�ľ������û�������ˮ�еĽ��弰�����������������ˮ�������dz�ȥˮ�н϶�ĸ����Ӻ�þ���ӣ�
�ʴ�Ϊ��ˮ�ľ������û�������ˮ�еĽ��弰�����������������ˮ�������dz�ȥˮ�н϶�ĸ����Ӻ�þ���ӣ�
��2����������ˮ���뱣֤��ȫ������ˮ����Ҫ��ȡ�Խ��Ӻ����еĵ�ˮ����ɱ���������������������˵ȹ��մ����������������ȷ˳���ǻ������������ˡ�ɱ���������ʴ�Ϊ���������������ˡ�ɱ��������
�ڸ��������ж����������ʿɵ��¶�����Ⱦ�����ܹ�����������ˮ����ɱ���������Ҳ�����ɶ�����Ⱦ��ֻ�г������ʴ�Ϊ��d��
��3���ٹ�ҵ�ϳ���������������������ȥ��Ȼˮ�к��е�������ͽ��壬Ϊ�˴ﵽ���õ�Ч����Ҫ��������ˮ��pH����9���ң��ټ��̷���ԭ��Fe2+�ڼ����������ױ�������Fe3+������ˮ������Fe��OH��3���壬�ϺõĻ������ã�4Fe2++O2+2H2O+8OH-=4Fe��OH��3�����壩��
�ʴ�Ϊ��Fe2+�ڼ����������ױ�������Fe3+������ˮ������Fe��OH��3���壬�ϺõĻ������ã�4Fe2++O2+2H2O+8OH-�T4Fe��OH��3�����壩��
����Fe��0H��3��ȡNa2FeO4�Ļ�ѧ����ʽΪ2Fe��OH��3+3NaClO+4NaOH�T2Na2FeO4+3NaCl+5H2O��
�ʴ�Ϊ��2Fe��OH��3+3NaClO+4NaOH�T2Na2FeO4+3NaCl+5H2O��
��4��Na2CO3��Һ��Ũ��Ϊ5.6��10-5mol/L���������Ϻ���Һ��c��CO32-��=
��5.6��10-5mol/L=2.8��10-5mol/L������Ksp=c��CO32-��?c��Ca2+��=2.8��10-9��֪��c��Ca2+��=
mol/L=1��10-4mol/L��ԭ��ҺCa��OH��2��Һ����СŨ��Ϊ�����Һ��c��Ca2+����2������ԭ��ҺCa��OH��2��Һ����СŨ��Ϊ2��1��10-4mol/L=2��10-4mol/L���ʴ�Ϊ��2��10-4mol/L��
�ʴ�Ϊ��ˮ�ľ������û�������ˮ�еĽ��弰�����������������ˮ�������dz�ȥˮ�н϶�ĸ����Ӻ�þ���ӣ�
��2����������ˮ���뱣֤��ȫ������ˮ����Ҫ��ȡ�Խ��Ӻ����еĵ�ˮ����ɱ���������������������˵ȹ��մ����������������ȷ˳���ǻ������������ˡ�ɱ���������ʴ�Ϊ���������������ˡ�ɱ��������
�ڸ��������ж����������ʿɵ��¶�����Ⱦ�����ܹ�����������ˮ����ɱ���������Ҳ�����ɶ�����Ⱦ��ֻ�г������ʴ�Ϊ��d��
��3���ٹ�ҵ�ϳ���������������������ȥ��Ȼˮ�к��е�������ͽ��壬Ϊ�˴ﵽ���õ�Ч����Ҫ��������ˮ��pH����9���ң��ټ��̷���ԭ��Fe2+�ڼ����������ױ�������Fe3+������ˮ������Fe��OH��3���壬�ϺõĻ������ã�4Fe2++O2+2H2O+8OH-=4Fe��OH��3�����壩��
�ʴ�Ϊ��Fe2+�ڼ����������ױ�������Fe3+������ˮ������Fe��OH��3���壬�ϺõĻ������ã�4Fe2++O2+2H2O+8OH-�T4Fe��OH��3�����壩��
����Fe��0H��3��ȡNa2FeO4�Ļ�ѧ����ʽΪ2Fe��OH��3+3NaClO+4NaOH�T2Na2FeO4+3NaCl+5H2O��
�ʴ�Ϊ��2Fe��OH��3+3NaClO+4NaOH�T2Na2FeO4+3NaCl+5H2O��
��4��Na2CO3��Һ��Ũ��Ϊ5.6��10-5mol/L���������Ϻ���Һ��c��CO32-��=
| 1 |
| 2 |
| 2.8��10-9 |
| 2.8��10-5 |
���������⿼����ۺϣ��漰���������ᴿ���ܶȻ��ļ��㡢������ԭ��Ӧ��Ӧ�õȣ�ע�ظ�Ƶ����Ŀ��飬�ۺ��Խ�ǿ����Ŀ�ѶȽϴ�ע�⻯ѧ���������ϵ��

��ϰ��ϵ�д�
�����Ŀ
�����ᡢ���ᡢ��������ᶼ��ǿ�ᣬ��������ˮ��Һ�в��������ij�¶������������ڱ������еĵ��볣���ӱ������ж�����˵���в���ȷ���ǣ�������
| �� | HClO4 | H2SO4 | HCl | HNO3 |
| Ka | 1.6��10-5 | 6.3��10-9 | 1.6��10-9 | 4.2��10-10 |
| A���ڱ��������������ᶼû����ȫ���� |
| B���ڱ������и�������������������ǿ���� |
| C���ڱ�����������ĵ��뷽��ʽΪH2SO4=2H++SO42- |
| D�����ǿ�����䱾���Ľṹ���ܼ��������й� |
���Ӻ������Լ�����ѧ��ѧ�г�����ʵ�飮��ʵ�鷽��������ȷ���ǣ�������
| A���������ᾧ����ȥKNO3��������NaCl |
| B���ü���NaOH��aq��������ķ�����ȥ��ȩ������������ |
| C��ȷ��ȡ14.800g Ca��OH��2������100mL 2.0 mol/L��Ca��OH��2��Һ |
| D����2mL10%��CuSO4��aq���е���3�� 2%��NaOH��aq�������Ƽ���ȩ�����Լ� |
�м��ᡢ������Ҷ�����ɵĻ����a g������ȫȼ�տ�����CO20.2mol����ȫ�к͵������ĸû��������80mL 2mol/L��NaOH��Һ����aֵ����Ϊ��������
| A��8.00 | B��7.92 |
| C��7.90 | D��7.86 |
��������5��ת�������в�����ͨ��һ����Ӧʵ�ֵ��ǣ�������
��Al2O3��Al����CuSO4-��CuCl2����SiO2-��H2SiO3 ����CuO-��Cu��OH��2����Na2O2-��NaOH��
��Al2O3��Al����CuSO4-��CuCl2����SiO2-��H2SiO3 ����CuO-��Cu��OH��2����Na2O2-��NaOH��
| A���٢� | B���ۢ� |
| C���ڢۢ� | D���ڢۢܢ� |
����������ȷ���ǣ�������
| A���������ӵ��������������Ӵ������� |
| B����FeCl2��Һ�еμ���ˮ����Һ��ɫ����ػ�ɫ��˵����ˮ�к���HClO |
| C����FeCl3��Һ�еμӹ�����ˮ������ȡFe��OH��3���� |
| D�����ۻ������������CuSO4��Һ��������˵�����Ľ���������ͭ |
��ӦC ��s��+CO2��g���T2CO��g���ں���������һ���¶��´ﵽƽ�⣬�ٳ���CO2���ﵽ�µ�ƽ��ʱ���¶Ȳ��䣩����ԭƽ��ȣ�������ȷ���ǣ�������
| A��ƽ��������Ӧ�����ƶ� |
| B����������ƽ��Ħ���������� |
| C��CO2��ת�������� |
| D������Ӧ���������淴Ӧ���ʼ�С |
��������CuO��MgO��ĩ�ֱ����������������еõ������ͬ��Ũ�ȷֱ�Ϊamol?L-1��bmol?L-1��Cu��NO3��2��Mg��NO3��2��Һ����a��b�Ĺ�ϵΪ��������
| A��2a=b | B��a=2b |
| C��a=b | D����ȷ�� |
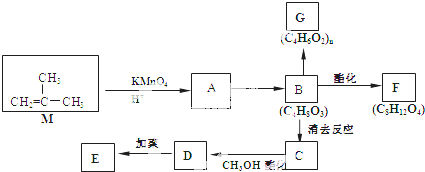
 �ṹ���л���ɱ����Ը��������Һ�����ɶ�Ԫ�����磺CH2=CH2
�ṹ���л���ɱ����Ը��������Һ�����ɶ�Ԫ�����磺CH2=CH2 ��Ϊԭ�Ϻϳɻ�״������F�߷��ӻ�����E��G��
��Ϊԭ�Ϻϳɻ�״������F�߷��ӻ�����E��G��