题目内容
下列叙述正确的是( )
| A、用锡焊接的铁质器件,焊接处易生锈 |
| B、向FeCl2溶液中滴加氯水,溶液颜色变成棕黄色,说明氯水中含有HClO |
| C、向饱和FeCl3溶液中滴加过量氨水,可制取Fe(OH)3胶体 |
| D、将钝化后的铝条放入CuSO4溶液中无现象,说明铝的金属性弱于铜 |
考点:铁盐和亚铁盐的相互转变,铁的化学性质
专题:元素及其化合物
分析:A.锡、铁和电解质溶液构成原电池,铁作负极而易被腐蚀;
B.向FeCl2溶液中滴加氯水,氯气与氯化亚铁反应生成氯化铁;
C.氯化铁与氨水反应生成氢氧化铁沉淀;
D.钝化后的铝条表面有一层致密的氧化膜,性质稳定.
B.向FeCl2溶液中滴加氯水,氯气与氯化亚铁反应生成氯化铁;
C.氯化铁与氨水反应生成氢氧化铁沉淀;
D.钝化后的铝条表面有一层致密的氧化膜,性质稳定.
解答:
解:A.锡、铁和电解质溶液构成原电池,铁作负极而易被腐蚀,故A正确;
B.向FeCl2溶液中滴加氯水,氯气与氯化亚铁反应生成氯化铁,氯化铁溶液为黄色,不能说明氯水中含有HClO,故B错误;
C.氯化铁与氨水反应生成氢氧化铁沉淀,得不到胶体,故C错误;
D.钝化后的铝条表面有一层致密的氧化膜,阻止铝与铜离子的接触,从而无明显现,不能说明铝的金属性弱于铜,故D错误;
故选:A.
B.向FeCl2溶液中滴加氯水,氯气与氯化亚铁反应生成氯化铁,氯化铁溶液为黄色,不能说明氯水中含有HClO,故B错误;
C.氯化铁与氨水反应生成氢氧化铁沉淀,得不到胶体,故C错误;
D.钝化后的铝条表面有一层致密的氧化膜,阻止铝与铜离子的接触,从而无明显现,不能说明铝的金属性弱于铜,故D错误;
故选:A.
点评:本题考查了元素化合物知识,熟悉原电池工作原理、氯气、次氯酸的性质、胶体的制备是解题关键,题目难度不大,注意对基础知识的积累.

练习册系列答案
相关题目
在一定条件下,HA溶液存在电离平衡:HA?H++A--Q.下列说法正确的是( )
| A、稀释溶液,HA电离平衡常数增大 |
| B、升高温度,HA电离程度增大 |
| C、加入NaA固体,平衡朝正反应方向移动 |
| D、加入NaOH固体,溶液pH减小 |
下列关于硫化氢或氢硫酸的描述,正确的是( )
| A、氢硫酸因含-2价的硫,所以只有还原性 |
| B、硫化氢气体通入硫酸亚铁中有黑色沉淀生成 |
| C、实验室制取硫酸氢时,可以用稀盐酸或稀硫酸,但不能用浓硫酸或硝酸 |
| D、氢硫酸溶液中加入镁粉会有氢气产生 |
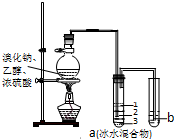 实验室制取少量溴乙烷的装置如图所示,将生成物导入盛有冰水混合物的试管a中,实验结束发现试管a中的物质分为三层.对该实验的分析错误的是( )
实验室制取少量溴乙烷的装置如图所示,将生成物导入盛有冰水混合物的试管a中,实验结束发现试管a中的物质分为三层.对该实验的分析错误的是( )| A、烧瓶中除发生取代反应可能发生消去反应、氧化还原反应等 |
| B、产物在a中第一层 |
| C、a中有产物和水还含HBr、CH3CH2OH等 |
| D、b中盛放的酸性KMnO4溶液会褪色 |
下列各组化合物中,不论二者以何种比例混合,只要总质量一定,则完全燃烧时生成的水的量与消耗氧气的量都相等的是( )
| A、HCHO、CH3CHO |
| B、C3H8、C3H8O |
| C、C2H2、C6H6 |
| D、CH4、C3H4 |




