题目内容
称取4.99g胆矾晶体(CuSO4.5H2O)溶于水制成100g溶液,并将所得溶液用惰性电极进行电解.电解一段时间后,测得阴极增重0.254g.问此时:
(1)阳极上一共产生了多少体积气体(标准状况)?
(2)留下的电解质溶液中,硫酸铜的质量分数是多少?
(1)阳极上一共产生了多少体积气体(标准状况)?
(2)留下的电解质溶液中,硫酸铜的质量分数是多少?
考点:电解原理
专题:电化学专题
分析:(1)阴极增重既是Cu质量,计算铜物质的量和加入硫酸铜晶体所含铜离子物质的量比较判断电解过程中,硫酸铜过量,依据电极反应过程中电子守恒计算阳极生成的气体物质的量,得到气体体积;
(2)计算电解的硫酸铜溶液生成铜和放出氧气质量得到剩余溶液质量,结合电解过程计算剩余硫酸铜质量,依据质量分数=
×100%计算得到.
(2)计算电解的硫酸铜溶液生成铜和放出氧气质量得到剩余溶液质量,结合电解过程计算剩余硫酸铜质量,依据质量分数=
| 溶质质量 |
| 溶液质量 |
解答:
解:(1)阴极增重既是Cu质量,物质的量=
=0.004mol,4.99g胆矾晶体(CuSO4.5H2O)物质的量=
=0.02mol.所以硫酸铜剩余,阳极只能产生O2,依据电子守恒,生成氧气与Cu等电子量=0.008mol,故氧气为
=0.002mol标准状况阳极气体体积=0.002mol×22.4L/mol=0.0448L=44.8ml,
答:阳极上一共产生了气体体积为44.8mL;
(2)硫酸铜剩余0.016mol,质量=0.016mol×159.5g/mol=2.552克,溶液为100g-0.254g-0.064g=99.62g,计算可得质量分数=
×100%=2.6%,
答:留下的电解质溶液中,硫酸铜的质量分数是2.6%.
| 0.254g |
| 63.5g/mol |
| 4.99g |
| 249.5g/mol |
| 0.008mol |
| 4 |
答:阳极上一共产生了气体体积为44.8mL;
(2)硫酸铜剩余0.016mol,质量=0.016mol×159.5g/mol=2.552克,溶液为100g-0.254g-0.064g=99.62g,计算可得质量分数=
| 2.552g |
| 99.62g |
答:留下的电解质溶液中,硫酸铜的质量分数是2.6%.
点评:本题考查了电解原理的分析应用,电极反应和电子守恒的计算分析,掌握基础是关键,题目难度中等.

练习册系列答案
 导学教程高中新课标系列答案
导学教程高中新课标系列答案
相关题目
下列实验与对应的图象符合的是( )
A、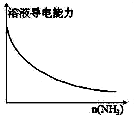 向一定量的CH3COOH溶液中通入NH3至过量 |
B、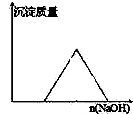 向等物质的量的HCl和AlCl3溶液中滴入NaOH溶液至过量 |
C、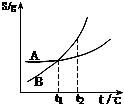 表示A、B两物质的溶解度随温度变化情况,将t1℃时A、B饱和溶液升温至t2℃时,溶质的质量分数B=A |
D、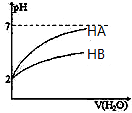 表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则同浓度的NaA溶液的pH大于NaB溶液 |
物质的量为0.20mol的镁条在只含有CO2和O2混合气体的容器中燃烧(产物不含碳酸镁),反应后容器内固体物质的质量不可能为( )
| A、6.4g | B、8.0g |
| C、8.4g | D、9.2g |

