题目内容
在一个固定容积的密闭容器中,加入2.0LX气体,和3.0LY气体,可发生可逆反应;nX(g)+3Y(g)![]() 2R(g)+U(g).当达到平衡时,测知X的转化率为30%,Y的转化率为60%,则在该反应中的n值是:
2R(g)+U(g).当达到平衡时,测知X的转化率为30%,Y的转化率为60%,则在该反应中的n值是:
[ ]
|
A.1 |
B.2 |
|
C.3 |
D.4 |
答案:A
解析:
解析:
|
此题可用化学反应速率之比等于计量系数之比解之,过程如下: nX(g)+3Y(g) 原 2.0 3.0 0 0 反应2×30% 3×60% 1.2 0.6 变化量之比为:n:3:2:1=0.6:1.8:1.2:0.6,故n=1. |

练习册系列答案
相关题目
在一个固定容积的密闭容器中,可发生以下反应:A(g)+B(g)?xC(g);△H=?符合下图(a)所示的关系,由此推断关于图(b)的说法正确的是( )
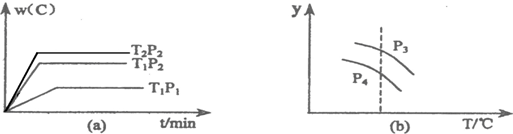

| A、P3>P4,y轴表示A的转化率 | B、P3<P4,y轴表示B的体积分数 | C、P3>P4,y轴表示混合气体的平均相对分子质量 | D、P3>P4,y轴表示混合气体的密度 |
在一个固定容积的密闭容器中,加入m mol A、n mol B,发生下列反应:mA(g)+nB(g)?pC(g),平衡时C的浓度是w mol/L,若容器体积和温度不变,起始时放入a mol A、b mol B、c mol C,若要平衡后C的浓度仍为w mol/L,则a、b、c应满足的关系是( )
| A、a:b:c=m:n:p | ||||||
B、a:b=m:n,
| ||||||
C、
| ||||||
D、a=
|
 2C(g),起始加入1molA和2molB,反应达到平衡后测得C的浓度为p mol/L,且C的体积分数为ω.在相同条件下:
2C(g),起始加入1molA和2molB,反应达到平衡后测得C的浓度为p mol/L,且C的体积分数为ω.在相同条件下: 2SO3(g),(正反应是放热反应),达到平衡后,其它条件不变时,只改变下列的某一个条件,将变化的情况(增大、减小、不变)填入空格中.
2SO3(g),(正反应是放热反应),达到平衡后,其它条件不变时,只改变下列的某一个条件,将变化的情况(增大、减小、不变)填入空格中. 化学学科中的平衡理论主要内容包括:化学平衡、电离平衡、水解平衡和溶解平衡等四种.且均符合勒夏特列原理.请回答下列问题.
化学学科中的平衡理论主要内容包括:化学平衡、电离平衡、水解平衡和溶解平衡等四种.且均符合勒夏特列原理.请回答下列问题.