题目内容
用下列装置能达到预期目的是( )
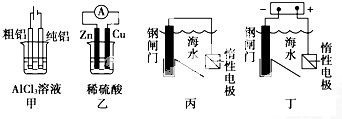

| A、甲图装置可用于电解精炼铝 |
| B、乙图装置可得到持续、稳定的电流 |
| C、丙图装置可达到保护钢闸门的目的 |
| D、丁图装置可达到保护钢闸门的目的 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:A、电解精炼铝可以让粗Al做阳极,精Al做阴极,电解质可以是熔融的氧化铝;
B、原电池可以产生电流但不能提供稳定的电流;
C、原电池的负极金属易被腐蚀;
D、电解池的阴极金属被保护,不易腐蚀.
B、原电池可以产生电流但不能提供稳定的电流;
C、原电池的负极金属易被腐蚀;
D、电解池的阴极金属被保护,不易腐蚀.
解答:
解:A、电解精炼铝可以让粗铝做阳极,精铝做阴极,电解质不能是氯化铝溶液,这样在阴极上会析出氢气,可以是熔融的氧化铝,故A错误;
B、原电池可以产生电流但不能提供稳定的电流,故B错误;
C、丙图装置中,形成原电池,钢闸门是负极,易被腐蚀,不能达到保护钢闸门的目的,故C错误;
D、丁图装置,形成电解池,钢闸门是阴极,不易被腐蚀,可达到保护钢闸门的目的,故D正确.
故选D.
B、原电池可以产生电流但不能提供稳定的电流,故B错误;
C、丙图装置中,形成原电池,钢闸门是负极,易被腐蚀,不能达到保护钢闸门的目的,故C错误;
D、丁图装置,形成电解池,钢闸门是阴极,不易被腐蚀,可达到保护钢闸门的目的,故D正确.
故选D.
点评:本题涉及原电池和电解池的工作原理的应用以及金属的防护和腐蚀方面的知识,注意知识的灵活应用是关键,难度中等.

练习册系列答案
相关题目
下列事实不能用平衡移动原理解释的是( )
| A、实验室中常用排饱和食盐水的方法收集氯气 |
| B、配制FeC13溶液时加入少量的盐酸 |
| C、实验室利用双氧水制备氧气时使用催化剂 |
| D、工业上生产硫酸的过程中使用过量的空气以提高二氧化硫的利用率 |
下列各组物质中,不满足组内任意两种物质在一定条件下均能发生反应的是( )
| 组别 | 甲 | 乙 | 丙 |
| A | Al(OH)3 | HCl | NaOH |
| B | NH3 | O2 | HNO3 |
| C | SO2 | Ca(OH)2 | NaHCO3 |
| D | O2 | N2 | H2 |
| A、A | B、B | C、C | D、D |
已知某气态烃1mol最多可与2molHCl发生加成反应,所得产物与Cl2发生取代反应时,若将氢原子全部取代,需要8mol Cl2,则该烃可能是( )
| A、丙炔 | B、乙炔 |
| C、2-丁炔 | D、2-丁烯 |
加热5.00g碳酸钠和碳酸氢钠的混合物,使碳酸氢钠完全分解,混合物质量减少了0.31g,则原混合物中碳酸钠的质量为( )
| A、3.38 g |
| B、4.58 g |
| C、4.41 g |
| D、4.16 g |
下列叙述中,不能用勒夏特列原理解释的是( )
| A、红棕色的NO2,加压后颜色先变深后变浅 |
| B、高压比常压有利于合成SO3的反应 |
| C、由H2、I2(g)、HI(g)气体组成的平衡体系加压后颜色变深 |
| D、实验室用排饱和食盐水的方法收集氯气 |