题目内容
在一个体积可变的密闭容器中,通入2molHI气体,在一定条件下建立如下平衡:2HI(g)?I2(g)+H2(g);△H>0,测得平衡时容器体积为1L,c(I2)=0.5mol/L.改变相关条件,下列结论正确的是( )
| A、保持容器体积不变,升高温度,混合气体的颜色逐渐变深 |
| B、恒温,恒容,充入一定量氦气(不参与反应),则正反应速率和逆反应速率均增大 |
| C、恒温,缓慢压缩容器,使容器体积恒定为0.2L,一定时间后,测得c(I2)=2.5mol/L |
| D、恒温、恒压,再通入2mol HI气体,到达平衡状态后,HI转化率会提高 |
考点:化学平衡的影响因素,化学平衡建立的过程
专题:化学平衡专题
分析:A.升高温度,平衡向正反应方向移动;
B.保持容器体积与温度不变,充入一定量氦气,反应物的浓度不变,速率不变;
C.反应前后两边气体的计量数相等,改变压强平衡不移动;
D.从等效平衡的角度,考虑转化率.
B.保持容器体积与温度不变,充入一定量氦气,反应物的浓度不变,速率不变;
C.反应前后两边气体的计量数相等,改变压强平衡不移动;
D.从等效平衡的角度,考虑转化率.
解答:
解:A.正反应吸热,升高温度,平衡向正反应方向移动,混合气体的颜色逐渐变深,故A正确;
B.保持容器体积与温度不变,充入一定量氦气,反应物的浓度不变,速率不变,故B错误;
C.反应前后两边气体的计量数相等,改变压强平衡不移动,使容器体积恒定为0.2L,I2的物质的量不变,则c(I2)=0.5mol/L×
=2.5mol/L,故C正确;
D.保持容器压强和温度不变,再通入2molHI气体,在恒压条件下与原平衡状态相同,为等效平衡,则HI的转化率不变,故D错误.
故选AC.
B.保持容器体积与温度不变,充入一定量氦气,反应物的浓度不变,速率不变,故B错误;
C.反应前后两边气体的计量数相等,改变压强平衡不移动,使容器体积恒定为0.2L,I2的物质的量不变,则c(I2)=0.5mol/L×
| 1L |
| 0.2L |
D.保持容器压强和温度不变,再通入2molHI气体,在恒压条件下与原平衡状态相同,为等效平衡,则HI的转化率不变,故D错误.
故选AC.
点评:本题考查化学平衡的计算,题目难度中等,本题易错点为D,注意从等效平衡的角度分析

练习册系列答案
 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案
相关题目
设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A、1L 1.0mol?L-1的NaC1O溶液中含有C1O-的数目为NA |
| B、标准状况下,22.4L盐酸含有NA个HC1分子 |
| C、常温常压下,14g由N2与CO组成的混合气体含有的原子数目为NA |
| D、1molNa被完成氧化生成Na2O2,失去个2NA电子 |
在同浓度的KHCO3和NH4HCO3溶液中,c(CO32-)和c(HCO3-)大的分别是( )
| A、KHCO3、NH4HCO3 |
| B、NH4HCO3、KHCO3 |
| C、KHCO3、KHCO3 |
| D、NH4HCO3、NH4HCO3 |
下列有关说法错误的是( )
| A、油脂的种类很多,但它们水解后都一定有一产物相同 | ||
| B、淀粉、纤维素都属糖类,它们通式相同,但它们不互为同分异构体 | ||
C、已知CH4+H2O
| ||
| D、C(CH3)4的二氯代物只有2种 |
NA表示阿伏加德罗常数的值,4℃时,25滴水为amL,则1滴水中含有的水分子数为( )
| A、aNA/25 |
| B、aNA/(25×18) |
| C、aNA/(25×20) |
| D、aNA/(1000×22.4) |
下列反应中,水作为氧化剂的是( )
| A、Cl2+H2O═HCl+HClO |
| B、2F2+H2O═4HF+O2 |
| C、2Na+2H2O═2 NaOH+H2↑ |
| D、SO3+H2O═H2SO4 |
将化合物分成电解质和非电解质的分类标准是( )
| A、溶于水后形成的溶液能否导电 |
| B、在熔化状态能不能电离 |
| C、在水中或熔化状态下能否电离 |
| D、在水溶液中能否电离 |
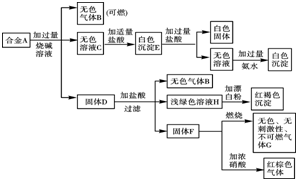 现有四种单质组成的合金A,为分析其成分,用此合金进行一系列实验,其过程及发生反应的现象如下图所示.
现有四种单质组成的合金A,为分析其成分,用此合金进行一系列实验,其过程及发生反应的现象如下图所示.