题目内容
15.下列有关反应中,属于吸热反应的是( )| A. | 碳酸钙受热分解 | B. | 天然气的燃烧 | ||
| C. | 铝粉与稀盐酸反应 | D. | 生石灰变成熟石灰 |
分析 根据常见的放热反应有:所有的物质燃烧、所有金属与酸反应、金属与水反应,所有中和反应、绝大多数化合反应和铝热反应;
常见的吸热反应有:绝大数分解反应,个别的化合反应(如C和CO2),少数分解置换以及某些复分解(如铵盐和强碱).
解答 解:A、碳酸钙在高温下的分解反应是吸热反应,故A正确;
B、天然气的燃烧反应放出大量的热,则属于放热反应,故B错误;
C、金属与酸的反应,属于放热反应,故C错误;
D、生石灰和水发生反应生成熟石灰,属于化合反应,为放热反应,故D错误.
故选A.
点评 本题考查吸热反应,抓住中学化学中常见的吸热或放热的反应是解题的关键,对于特殊过程中的热量变化的要熟练记忆来解答此类习题.

练习册系列答案
 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案 黄冈创优卷系列答案
黄冈创优卷系列答案
相关题目
5.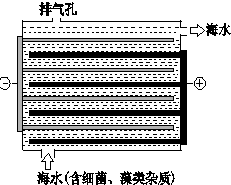 海洋化学资源的研究和合理利用具有广阔前景,从海水中可提取氯、溴、碘等卤族元素.
海洋化学资源的研究和合理利用具有广阔前景,从海水中可提取氯、溴、碘等卤族元素.
(1)氯原子结构示意图是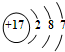 ,碘在元素周期表中的位置是第五周期ⅦA族,HI的稳定性比HBr弱(填写“强”或“弱”).
,碘在元素周期表中的位置是第五周期ⅦA族,HI的稳定性比HBr弱(填写“强”或“弱”).
(2)向浓缩的海水中通入Cl2,可将Br-转化为Br2.再用“空气吹出法”将Br2从浓海水中吹出,并用纯碱浓溶液吸收,生成NaBr、NaBrO3等.当有1mol Br2被纯碱吸收时,转移的电子数为1×1024.
(3)如图是NaClO的发生装置.该装置主要利用了电解饱和食盐水的原理,可实现对海水的消毒和灭藻.
①写出装置中产生NaClO的化学方程式2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$2NaOH+H2↑+Cl2↑,2NaOH+Cl2→NaClO+NaCl+H2O.
海水中含有Ca2+、Mg2+、HCO3-等杂质离子,处理过程中装置的阴极易产生水垢,其主要成分是Mg(OH)2和CaCO3.生成CaCO3的离子方程式是Ca2++HCO3-+OH-→CaCO3↓+H2O.
若每隔5-10min倒换一次电极电性,可有效地解决阴极的结垢问题.试用电极反应式并结合必要的文字进行解释阴极结垢后倒换电极电性,阴极变为阳极,其电极反应为:2Cl--2e→Cl2↑,产生的氯气与水发生反应:Cl2+H2=HCl+HClO,使该电极附近溶液呈酸性,从而将Mg(OH)2和CaCO3溶解而达到除垢的目的.
NaOH溶液吸收SO2得Na2SO3,可用Na2SO3吸收SO2.在SO2被吸收的过程中,pH随n(SO32-)、n(HSO3-)变化关系如下:
②从上表可判断,NaHSO3溶液呈酸性(填“酸性”、“碱性”、“中性”),请用平衡原理解释:HSO3-存在HSO3-?H++SO32-和HSO3-+H2O?H2SO3+OH-,HSO3-的电离程度大于水解程度.
③当吸收液呈中性时,溶液中离子浓度关系正确的是ab(选填字母).
a.c(Na+)=2c(SO32-)+c(HSO3-)
b.c(Na+)>c(HSO3-)>c(SO32-)>c(H+)=c(OH-)
c.c(Na+)+c(H+)=c(SO32-)+c(HSO3-)+c(OH-)
d.c(Na+)>c(SO32-)>c(HSO3-)>c(H+)=c(OH-)
 海洋化学资源的研究和合理利用具有广阔前景,从海水中可提取氯、溴、碘等卤族元素.
海洋化学资源的研究和合理利用具有广阔前景,从海水中可提取氯、溴、碘等卤族元素.(1)氯原子结构示意图是
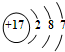 ,碘在元素周期表中的位置是第五周期ⅦA族,HI的稳定性比HBr弱(填写“强”或“弱”).
,碘在元素周期表中的位置是第五周期ⅦA族,HI的稳定性比HBr弱(填写“强”或“弱”).(2)向浓缩的海水中通入Cl2,可将Br-转化为Br2.再用“空气吹出法”将Br2从浓海水中吹出,并用纯碱浓溶液吸收,生成NaBr、NaBrO3等.当有1mol Br2被纯碱吸收时,转移的电子数为1×1024.
(3)如图是NaClO的发生装置.该装置主要利用了电解饱和食盐水的原理,可实现对海水的消毒和灭藻.
①写出装置中产生NaClO的化学方程式2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$2NaOH+H2↑+Cl2↑,2NaOH+Cl2→NaClO+NaCl+H2O.
海水中含有Ca2+、Mg2+、HCO3-等杂质离子,处理过程中装置的阴极易产生水垢,其主要成分是Mg(OH)2和CaCO3.生成CaCO3的离子方程式是Ca2++HCO3-+OH-→CaCO3↓+H2O.
若每隔5-10min倒换一次电极电性,可有效地解决阴极的结垢问题.试用电极反应式并结合必要的文字进行解释阴极结垢后倒换电极电性,阴极变为阳极,其电极反应为:2Cl--2e→Cl2↑,产生的氯气与水发生反应:Cl2+H2=HCl+HClO,使该电极附近溶液呈酸性,从而将Mg(OH)2和CaCO3溶解而达到除垢的目的.
NaOH溶液吸收SO2得Na2SO3,可用Na2SO3吸收SO2.在SO2被吸收的过程中,pH随n(SO32-)、n(HSO3-)变化关系如下:
| n(SO32-):n(HSO3-) | 91:9 | 1:1 | 1:91 |
| pH | 8.2 | 7.2 | 6.2 |
③当吸收液呈中性时,溶液中离子浓度关系正确的是ab(选填字母).
a.c(Na+)=2c(SO32-)+c(HSO3-)
b.c(Na+)>c(HSO3-)>c(SO32-)>c(H+)=c(OH-)
c.c(Na+)+c(H+)=c(SO32-)+c(HSO3-)+c(OH-)
d.c(Na+)>c(SO32-)>c(HSO3-)>c(H+)=c(OH-)
6.若NA表示阿伏加德罗常数,下列说法正确的是( )
| A. | 在标准状况下,NA个水分子所占的体积约为22.4L | |
| B. | 5.6g铁与氯气完全反应,失去电子的数目为0.2NA | |
| C. | 1mol C12发生化学反应,转移的电子数一定为2NA | |
| D. | 在标准状况下,22.4L由N2、N2O组成的混合气体中所含有的氮原子为2NA |
3.下列离子方程式书写正确的是( )
| A. | 铁片粉与稀硝酸反应:Fe+2H+═Fe2++H2↑ | |
| B. | 氧化亚铁粉末溶于盐酸中:Fe2O3+6H+═2Fe3++3H2O | |
| C. | 铜与氯化铁溶液反应:2Fe3++Cu═2Fe2++Cu2+ | |
| D. | 向硫酸铝溶液中加入过量氨水:Al3++4OH-═AlO2+2H2O |


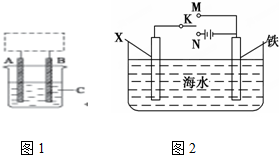 (I)研究CO2的利用对促进低碳社会的构建具有重要的意义.将CO2与焦炭作用生成CO,CO可用于炼铁等.
(I)研究CO2的利用对促进低碳社会的构建具有重要的意义.将CO2与焦炭作用生成CO,CO可用于炼铁等.