题目内容
17.硫在白然界中以游离态和多种化合态形成出现.硫的化合物大多具有氧化性或还原性.许多金属硫化物难溶于水.完成下列填空:(1)(1)硫化氢具有还原性,可以和许多氧化剂反应.在酸性条件下,H2S和KMnO4反应生成S、MnSO4、K2SO4和H2O,写出该反应的化学方程式.3H2SO4+5H2S+2KMnO4=5S↓+2MnSO4+K2SO4+8H2O.
(2)室温下,0.1mol/L的硫化钠溶液和0.1mol.L的碳酸钠溶液,碱性更强的是硫化钠溶液,其原因是硫氢根离子的电离常数小于碳酸氢根离子,则其水解程度大于碳酸根离子.
已知:H2S:Ka1=1.3×10-7 Ka2=7.1×10-15 H2CO3:Ka1=4.3×10-7 Ka2=5.6×10-11
(3)将黑色的Fe2S3固体加入足量盐酸中,溶液中有淡黄色固体生成,产物还有氯化亚铁、硫化氢.过滤,微热滤液,然后加入过量的氢氧化钠溶液,可观察到的现象是产生白色絮状沉淀,迅速变为灰绿色,最终变为红褐色沉淀.
分析 (1)H2S和KMnO4反应生成S、MnSO4、K2SO4和H2O,结合原子守恒书写化学方程式;
(2)电离常数越小,对应的盐溶液的碱性越强;
(3)将黑色的Fe2S3固体加入足量的盐酸中,生成H2S和氯化铁,氯化铁可氧化H2S生成S,加入氢氧化钠,可生成氢氧化亚铁,氢氧化亚铁被氧化生成氢氧化铁.
解答 解:(1)H2S和KMnO4反应生成S、MnSO4、K2SO4和H2O,反应的方程式为3H2SO4+5H2S+2KMnO4=5S↓+2MnSO4+K2SO4+8H2O,
故答案为:3H2SO4+5H2S+2KMnO4=5S↓+2MnSO4+K2SO4+8H2O;
(2)H2S第二步电离常数最小,则硫化钠易水解,溶液的碱性较强,
故答案为:硫化钠溶液;硫氢根离子的电离常数小于碳酸氢根离子,则其水解程度大于碳酸根离子;
(3)将黑色的Fe2S3固体加入足量的盐酸中,生成H2S和氯化铁,氯化铁可氧化H2S生成S,加入氢氧化钠,可生成氢氧化亚铁,氢氧化亚铁被氧化生成氢氧化铁,可观察到产生白色絮状沉淀,迅速变为灰绿色,最终变为红褐色沉淀,
故答案为:氯化亚铁、硫化氢;产生白色絮状沉淀,迅速变为灰绿色,最终变为红褐色沉淀.
点评 本题为2014年上海考题改编题,考查含硫物质的综合应用,弱电解质的电离等知识,侧重于学生的分析能力的考查,注意相关知识的积累,难度中等.

练习册系列答案
相关题目
5.Ⅰ.向FeCl3溶液中加入铁粉和铜粉混合粉末,充分反应后,分析溶液中的溶质和可能残留固体不溶物的成分.
(1)请完成下列表格
Ⅱ.今有一包铁粉和铜粉混合粉末,为确定其组成,现提供4mol/L的FeCl3溶液(其他用品略),某课外活动小组同学的实验结果如下(假定反应前后溶液体积不变).
(2)试判断第④组剩余固体质量x为0.第②组实验中,发生反应的离子方程式为2Fe3++Fe=3Fe2+.
(3)通过计算判断第②组剩余固体的成分.
(4)求原混合粉末中Fe、Cu的物质的量之比.
(1)请完成下列表格
| 序号 | 溶液中的盐 | 固体不溶物的成分 |
| ① | FeCl2、CuCl2、FeCl3 | |
| ② | 无 | |
| ③ | FeCl2、CuCl2 | |
| ④ | Cu | |
| ⑤ | Fe、Cu |
| 组别 | ① | ② | ③ | ④ |
| 混合粉末质量/g | 40 | 40 | 40 | 40 |
| FeCl3溶液体积/mL | 150 | 300 | 330 | 350 |
| 反应后剩余固体质量/g | 23.2 | 6.4 | 2.56 | x |
(3)通过计算判断第②组剩余固体的成分.
(4)求原混合粉末中Fe、Cu的物质的量之比.
8.已知CO2、BF3、SO3都是非极性分子,NH3、H2S、H2O、SO2都是极性分子,由此可推知ABn型分子是非极性分子的经验规律是( )
| A. | 分子中所有原子在同一平面 | |
| B. | 在ABn型分子中,A原子最外层电子不一定都成键 | |
| C. | 在ABn分子中,A元素为最高正价 | |
| D. | 分子中不含氢原子 |
12.将铝粉,石墨,二氧化钛按一定比例混合均匀,涂在金属表面,在高温下煅烧:4Al+3C+3TiO2=3TiC+2Al2O3
留在金属表面的涂层是一种高温金属陶瓷,广泛应用于火箭和导弹技术中.关于该反应,说法正确的是( )
留在金属表面的涂层是一种高温金属陶瓷,广泛应用于火箭和导弹技术中.关于该反应,说法正确的是( )
| A. | TiC中钛元素-4价 | B. | 每生成1molTiC转移电子4mol | ||
| C. | TiO2是氧化剂,Al,C是还原剂 | D. | TiC不属于新型无机非金属材料 |
6.不能用来说明金属X比金属Y还原性强的是( )
| A. | 把X和Y组成的合金放于潮湿的空气中,X先被腐蚀 | |
| B. | X原子最外层电子数比Y原子最外层电子数少 | |
| C. | X能从Y的盐溶液中把Y置换出来 | |
| D. | X的最高价氧化物的水化物碱性比Y的强 |
7.下列有关有机物分离提纯的方法正确的是( )
| A. | 溴苯中混有溴,加入KI溶液,振荡,用汽油萃取出I2 | |
| B. | 乙烷中混有乙烯,通过氢气在一定条件下反应,使乙烯转化为乙烷 | |
| C. | 乙烯中混有CO2和SO2,将其通过盛有NaOH溶液的洗气瓶,再干燥 | |
| D. | 除去乙醇中的微量水可加入金属钠,使其完全反应 |
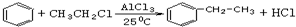
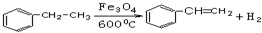 ;试以乙烯、苯、食盐、水等为原料制备苯乙醇 (
;试以乙烯、苯、食盐、水等为原料制备苯乙醇 (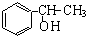 ),写出各步反应的化学方程式:
),写出各步反应的化学方程式: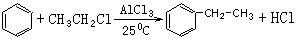 ;
;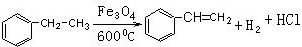 ;
;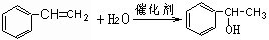 .
.