题目内容
6.使用容量瓶配制溶液,下列操作不正确的是( )| A. | 使用容量瓶前检查它是否漏水 | |
| B. | 容量瓶用蒸馏水洗净后,再用待配溶液润洗 | |
| C. | 盖好瓶塞,用食指顶住瓶塞,用另一只手指托住瓶底,把容量瓶倒转和摇动几次 | |
| D. | 容量瓶不能长期存放配制好的溶液 |
分析 A.容量瓶有瓶塞,使用前需要检查是否漏水;
B.不能用待测液润洗容量瓶,否则配制的溶液中溶质的物质的量偏大;
C.根据摇匀容量瓶的操作方法偏大;
D.容量瓶是用于配制一定物质的量浓度的溶液的仪器,不能长期盛放溶液.
解答 解:A.容量瓶有瓶塞,若漏水会影响配制结果,所以使用前需要检查容量瓶是否漏水,故A正确;
B.容量瓶用蒸馏水洗净后,不能用待测液润洗,否则会影响配制结果,故B错误;
C.为了使溶液均匀,正确操作方法为:盖好瓶塞,用食指顶住瓶塞,用另一只手指托住瓶底,把容量瓶倒转和摇动几次,该操作方法合理,故C正确;
D.盛放溶液应该选用相应的试剂瓶,容量瓶不能长期存放配制好的溶液,故D正确;
故选B.
点评 本题考查了容量瓶的使用方法,题目难度不大,明确配制一定物质的量浓度的溶液方法为解答关键,注意掌握容量瓶的构造及使用方法,试题培养了学生的分析能力及化学实验能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
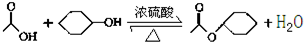
11.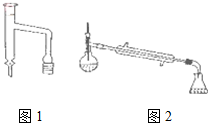 乙酸环己酯具有香蕉及苹果气味,主要用于配制各种饮料、冰淇淋等,实验室制备乙酸环己酯的反应原理、装置示意图和有关数据如下:
乙酸环己酯具有香蕉及苹果气味,主要用于配制各种饮料、冰淇淋等,实验室制备乙酸环己酯的反应原理、装置示意图和有关数据如下:
实验步骤:
将12.0g(0.2mol)乙酸、l0.0g(0.1mol)环己醇和15mL环己烷加入装有温度计、恒压滴液漏斗和球形冷凝管的四颈烧瓶中,在搅拌下,慢慢滴加15mL 98%浓硫酸,滴加完后将恒压滴液漏斗换成分水器装置,加热回流90min后,向反应液中依次加入水、10%的NaHCO3溶液、水洗涤,然后加无水MgSO4,放置过夜,加热蒸馏,收集168-174℃的馏分,得到无色透明、有香味的液体产品6.9g
(1)上述反应装置图中存在的一处错误是冷凝水应从下口进上口出.
(2)实验中控制乙酸的物质的量是环己醇的2倍,其目的是提高环已醇的转化率.
(3)分水器(图1)的作用是将生成的水及时从体系中分离出来,提高反应物的转化率.
(4)用l0%的NaHCO3溶液洗涤的目的是洗去硫酸和醋酸;第二次水洗的目的是洗去碳酸氢钠;加入无水MgSO4的目的是干燥.
(5)本次实验的产率为48.6%.(保留3位有效数字)
(6)若在进行蒸馏操作时,采用图2装置,会使实验的产率偏高
(填“偏高”或“偏低”),其原因是产品中会收集到未反应的环己醇.
 乙酸环己酯具有香蕉及苹果气味,主要用于配制各种饮料、冰淇淋等,实验室制备乙酸环己酯的反应原理、装置示意图和有关数据如下:
乙酸环己酯具有香蕉及苹果气味,主要用于配制各种饮料、冰淇淋等,实验室制备乙酸环己酯的反应原理、装置示意图和有关数据如下:
 | 相对分子质量 | 密度/g•cm-3 | 沸点 | 水中溶解性 | |
| 乙酸 | 60 | 1.051 | 118.0 | 溶 | |
| 环己醇 | 100 | 0.962 | 160.8 | 微溶 | |
| 乙酸环己酯 | 142 | 0.969 | 173.5 | 难溶 |
将12.0g(0.2mol)乙酸、l0.0g(0.1mol)环己醇和15mL环己烷加入装有温度计、恒压滴液漏斗和球形冷凝管的四颈烧瓶中,在搅拌下,慢慢滴加15mL 98%浓硫酸,滴加完后将恒压滴液漏斗换成分水器装置,加热回流90min后,向反应液中依次加入水、10%的NaHCO3溶液、水洗涤,然后加无水MgSO4,放置过夜,加热蒸馏,收集168-174℃的馏分,得到无色透明、有香味的液体产品6.9g
(1)上述反应装置图中存在的一处错误是冷凝水应从下口进上口出.
(2)实验中控制乙酸的物质的量是环己醇的2倍,其目的是提高环已醇的转化率.
(3)分水器(图1)的作用是将生成的水及时从体系中分离出来,提高反应物的转化率.
(4)用l0%的NaHCO3溶液洗涤的目的是洗去硫酸和醋酸;第二次水洗的目的是洗去碳酸氢钠;加入无水MgSO4的目的是干燥.
(5)本次实验的产率为48.6%.(保留3位有效数字)
(6)若在进行蒸馏操作时,采用图2装置,会使实验的产率偏高
(填“偏高”或“偏低”),其原因是产品中会收集到未反应的环己醇.
18.下列物质属于纯净物的是( )
| A. | 水泥 | B. | 不锈钢 | C. | 普 通玻璃 | D. | 液氯 |
15.有A、B、C、D四种强电解质,它们在水中电离产生系列离子(每种物质只含一种阴离子且互不重复).
已知:①A、C溶液的pH均大于7;
②一定浓度的A、B的溶液中水的电离程度可以相同;
③C溶液和D溶液相遇时只生成白色沉淀;
④仅B溶液和C溶液相遇时只生成刺激性气味的气体;
⑤A溶液和D溶液混合时无现象.
(1)写出A物质中所含化学键的类型离子键、共价键(或离子键、极性键和非极性键).
(2)写出C和D反应的离子方程式Ba2++SO42-=BaSO4↓.
(3)25℃时,0.1mol•L-1B溶液的pH=a,则B溶液中c(H+)-c(NH3•H20)=10 a-14(用含有a的关系式表示).
(4)将等体积、等物质的量浓度的B溶液和C溶液混合,反应后溶液中各种离子浓度由大到小的顺序是c(OH-)>c(Ba2+)=c(Cl-)>c(NH4+)>c(H+).
(5)25℃时,在一定体积的0.01mol•L-1的C溶液中,加入一定体积的0.01mol•L-1的盐酸,混合溶液的pH=12,若反应后溶液的体积等于C溶液与盐酸的体积之和,则C溶液与盐酸的体积比是2:1.
| 阳离子 | Na+、Ba2+、NH4+ |
| 阴离子 | CH3COO-、Cl-、OH-、SO42- |
②一定浓度的A、B的溶液中水的电离程度可以相同;
③C溶液和D溶液相遇时只生成白色沉淀;
④仅B溶液和C溶液相遇时只生成刺激性气味的气体;
⑤A溶液和D溶液混合时无现象.
(1)写出A物质中所含化学键的类型离子键、共价键(或离子键、极性键和非极性键).
(2)写出C和D反应的离子方程式Ba2++SO42-=BaSO4↓.
(3)25℃时,0.1mol•L-1B溶液的pH=a,则B溶液中c(H+)-c(NH3•H20)=10 a-14(用含有a的关系式表示).
(4)将等体积、等物质的量浓度的B溶液和C溶液混合,反应后溶液中各种离子浓度由大到小的顺序是c(OH-)>c(Ba2+)=c(Cl-)>c(NH4+)>c(H+).
(5)25℃时,在一定体积的0.01mol•L-1的C溶液中,加入一定体积的0.01mol•L-1的盐酸,混合溶液的pH=12,若反应后溶液的体积等于C溶液与盐酸的体积之和,则C溶液与盐酸的体积比是2:1.
16.下列物质按纯净物、混合物、电解质、非电解质顺序组合正确的一组为( )
| A. | 浓硫酸、空气、小苏打、乙醇 | B. | 生石灰、漂白粉、铁、二氧化硫 | ||
| C. | 明矾、盐酸、碳酸钙、氯气 | D. | 冰水混合物、氨水、纯碱、干冰 |
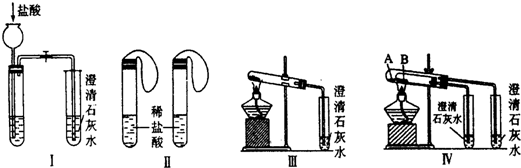
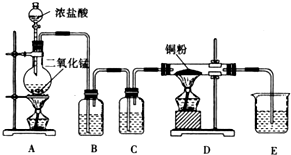 某实验学习小组用MnO2和浓盐酸制取纯净干燥的氯气,并让氯气与铜粉反应制取纯净的无水CuCl2,装置如图所示.
某实验学习小组用MnO2和浓盐酸制取纯净干燥的氯气,并让氯气与铜粉反应制取纯净的无水CuCl2,装置如图所示.