题目内容
写出下列反应并指明反应类型 (有机物用结构简式表示)
①由乙烯制乙醇
②实验室制甲烷
③乙烯使溴水褪色
④由乙烯制聚乙烯
⑤乙烷与氯气光照(第一步) .
①由乙烯制乙醇
②实验室制甲烷
③乙烯使溴水褪色
④由乙烯制聚乙烯
⑤乙烷与氯气光照(第一步)
考点:有机化学反应的综合应用
专题:有机反应
分析:①乙烯和水加成生成乙醇;
②实验室可采用加热无水醋酸钠和碱石灰的固体混合物的方法来制取甲烷;
③乙烯易和溴加成;
④乙烯中含有双键,发生加聚反应生成聚乙烯;
⑤乙烷与氯气发生取代反应生成氯乙烷和HCl.
②实验室可采用加热无水醋酸钠和碱石灰的固体混合物的方法来制取甲烷;
③乙烯易和溴加成;
④乙烯中含有双键,发生加聚反应生成聚乙烯;
⑤乙烷与氯气发生取代反应生成氯乙烷和HCl.
解答:
解:①乙烯含有双键,可以和水发生加成反应生成乙醇,方程式为:CH2=CH2 +H2O
CH3CH2OH,故答案为:CH2=CH2 +H2O
CH3CH2OH,加成反应;
②实验室可采用加热无水醋酸钠和碱石灰的固体混合物的方法来制取甲烷,反应方程式为:CH3COONa+NaOH
Na2CO3+CH4↑,故答案为:CH3COONa+NaOH
Na2CO3+CH4↑,取代反应;
③乙烯易和溴加成生成1,2-二溴乙烷,即CH2=CH2+Br-Br→CH2Br-CH2Br,故答案为:CH2=CH2+Br-Br→CH2Br-CH2Br,加成反应;
④乙烯中含有双键,发生加聚反应生成聚乙烯,该反应 ,
,
故答案为: ,加聚反应;
,加聚反应;
⑤乙烷与氯气发生取代反应生成氯乙烷和HCl,该反应为C2H6+Cl2
C2H5Cl+HCl,故答案为:C2H6+Cl2
C2H5Cl+HCl,取代反应.
| 催化剂 |
| △ |
| 催化剂 |
| △ |
②实验室可采用加热无水醋酸钠和碱石灰的固体混合物的方法来制取甲烷,反应方程式为:CH3COONa+NaOH
| CaO |
| △ |
| CaO |
| △ |
③乙烯易和溴加成生成1,2-二溴乙烷,即CH2=CH2+Br-Br→CH2Br-CH2Br,故答案为:CH2=CH2+Br-Br→CH2Br-CH2Br,加成反应;
④乙烯中含有双键,发生加聚反应生成聚乙烯,该反应
 ,
,故答案为:
 ,加聚反应;
,加聚反应;⑤乙烷与氯气发生取代反应生成氯乙烷和HCl,该反应为C2H6+Cl2
| 光照 |
| 光照 |
点评:本题考查有机物乙烯和乙烷的化学性质及甲烷的制取以及方程式的书写,可以根据所学知识进行回答,较简单.

练习册系列答案
相关题目
NaCl的摩尔质量是( )
| A、58.5 |
| B、58.5g |
| C、58.5g/mol |
| D、58.5mol |
关于金刚石、石墨和C60的判断,正确的是( )
| A、均含共价键 |
| B、互为同分异构体 |
| C、互为同位素 |
| D、性质相同 |
还原沉淀法是处理含铬(含Cr2072-和CrO42-)工业废水的常用方法,过程如下:CrO
Cr2O
Cr 3+
Cr(OH)3↓已知转化过程中的反应为:2CrO
(aq)+2H+ (aq)?Cr2O
(aq)+H2O(l).转化后所得溶液中铬元素的含量为28.6g/L,CrO42-有
转化为Cr2072-,下列说法不正确的是( )
2- 4 |
| H+ |
| 转换 |
2- 7 |
| Fe2+ |
| 还原 |
| OH- |
| 沉淀 |
2- 4 |
2- 7 |
| 10 |
| 11 |
| A、溶液颜色保持不变,说明上述可逆反应达到平衡状态 |
| B、若用绿矾(FeS04?7H20)(M=278)作还原剂,处理1 L废水,至少需要917.4 g |
| C、常温下转化反应的平衡常数K=1×1014,则转化后所得溶液的pH=6 |
| D、常温下Ksp[Cr(OH)3]=1×10-32,要使处理后废水中的c(Cr3+)降至1×10-5mol/L,应调溶液的pH=5 |
把NaHCO3和Na2CO3.10H2O混合6.56克溶于水,制成100ml溶液,其中Na+物质的量浓度为0.5mol/L,若将等质量的该混合物加热至恒重,所得固体质量为( )
| A、2.65 g |
| B、3.91 g |
| C、5.3 g |
| D、4.23g |
 ,Y为-OH、-OR、-X(卤原子)、-NH2等.格林试剂是有机合成中用途甚广的一种试剂,它可以与羰基加成,发生反应:
,Y为-OH、-OR、-X(卤原子)、-NH2等.格林试剂是有机合成中用途甚广的一种试剂,它可以与羰基加成,发生反应:


 卡托普列(Captopril)临床用于治疗高血压和充血性心力衰竭.它最有价值的合成路线为:
卡托普列(Captopril)临床用于治疗高血压和充血性心力衰竭.它最有价值的合成路线为: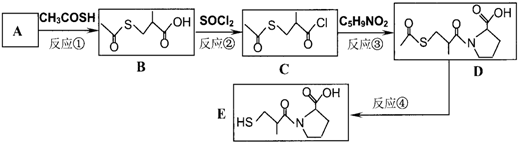
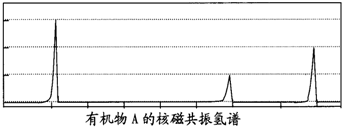
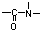 能在碱性条件下水解.则1molE最多能与
能在碱性条件下水解.则1molE最多能与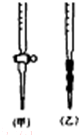 阅读下列实验内容,根据题目要求回答问题.
阅读下列实验内容,根据题目要求回答问题.