题目内容
15.用酸性氢氧燃料电池为电源进行电解的实验装置如图所示.下列说法中正确的是( )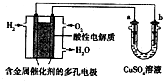
| A. | 燃料电池工作时,正极反应为:O2+4H++4e-═2H2O | |
| B. | a极是铁,b极是铜时,b极逐渐溶解,a极上有铜析出 | |
| C. | a极是纯铜,b极是粗铜时,可以达到铜的精炼目的 | |
| D. | a、b两极均是石墨时,在相同条件下a极产生的气体与电池中消耗的H2体积相等 |
分析 左边装置是氢氧燃料电池,所以是原电池,原电池放电时,燃料失电子发生氧化反应,所以投放燃料的电极为负极,投放氧化剂的电极为正极,正极上氧化剂得电子发生还原反应,由于电解质溶液呈酸性,正极反应为:O2+4e-+4H+=2H2O;右边装置有外接电源,所以是电解池,连接负极的b电极是阴极,连接正极的a电极是阳极,阳极上失电子发生氧化反应,阴极上得电子发生还原反应,结合电解反应解答.
解答 解:A.因该燃料电池是在酸性电解质中工作,所以正极反应为:O2+4e-+4H+=2H2O,故A正确;
B.a与电池正极相连,a为电解池阳极,b与电池的负极相连,b为电解池阴极,所以应该是a极的Cu溶解,b极上析出Cu,故B错误;
C.a极是粗铜,b极是纯铜时,为粗铜的精炼,电解时,a极逐渐溶解,b极上有铜析出,不符合精炼铜原理,故C错误;
D.电解CuSO4溶液时,a极产生的气体为O2,产生1molO2需4mol电子,所以需要燃料电池的2molH2,二者的体积并不相等,故D错误;
故选A.
点评 本题考查原电池和电解池知识,题目难度中等,易错点为B,注意电解质的酸碱性,为解答该题的关键.

练习册系列答案
相关题目
5.已知NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l);△H=-57.3kJ/mol,下列说法中正确的是( )
| A. | 浓硫酸和NaOH溶液反应,生成 l mol水时放热57.3 kJ | |
| B. | 含l molH2SO4的稀硫酸与足量稀NaOH溶液中和后,放热为57.3 kJ | |
| C. | 1L 0.l mol/L CH3COOH与1L 0.l mol/L NaOH溶液反应后放热为5.73 kJ | |
| D. | 1L 0.l mol/L HNO3与 1L 0.l mol/L NaOH溶液反应后放热为 5.73 kJ |
10.下列有机化合物中均含有杂质.除去这些杂质的方法和对应原理都正确的是( )
| 选项 | 杂质方法 | 除杂方法 | 原理 |
| A | 苯中含苯酚杂质 | 加入浓溴水,过滤 | 苯酚能与溴水反应生成白色沉淀 |
| B | 乙酸乙酯中含乙酸杂质 | 加饱和Na2CO3溶液洗涤,分液 | 乙酸乙酯在饱和Na2CO3溶液中的溶解度小且乙酸与Na2CO3反应 |
| C | 除去溴苯中的苯 | 蒸馏 | 苯的沸点比溴苯高 |
| D | 乙醇中含乙酸杂质 | 加入饱和Na2CO3溶液洗涤,分液 | 乙酸能与Na2CO3反应 |
| A. | A | B. | B | C. | C | D. | D |
13.溴苯是一种重要的化工原料,实验室合成溴苯的装置示意图及有关数据如图:
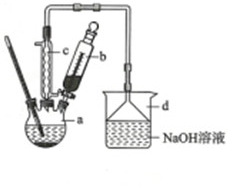
回答下列问题:
(1)在a中加入12mL无水苯和少量铁屑.在b中加入8.0mL液溴,向a中滴入几滴溴,有白雾产生,是因为生成了HBr气体,继续滴加至液溴滴完.装置d的作用是吸收HBr和Br2;
其中发生反应的离子方程式是H++OH-=H2O等(写出一个即可).
(2)上述装置图中,c的名称是冷凝管.
(3)液溴滴完后,经过下列步骤分离提纯:
①向a中加入10mL水,然后过滤除去未反应的铁屑;
②滤液依次用10mL水、8mL10%的NaOH溶液、10mL水洗涤.NaOH溶液洗涤的作用是除去HBr和未反应的Br2;
③向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤.加入氯化钙的目的是干燥.
(4)经以上分离操作后,粗溴苯中还含有的主要杂质为苯,要进一步提纯,还要进行的操作是C(填字母序号).
A.重结晶 B.过滤 C.蒸馏 D.萃取
(5)该实验中,a的容积最适合的是B(填字母序号).
A.25mL B.50mL C.250mL D.500mL.
(6)在该实验中最终制得的纯净溴苯质量为15.7g,则该实验中溴苯的产率为73.85%%(精确到小数点后一位).
| 苯 | 溴 | 溴苯 | |
| 密度/g•cm-3 | 0.88 | 3.10 | 1.50 |
| 沸点/℃ | 80 | 59 | 156 |
| 水中溶解度 | 微溶 | 微溶 | 微溶 |

回答下列问题:
(1)在a中加入12mL无水苯和少量铁屑.在b中加入8.0mL液溴,向a中滴入几滴溴,有白雾产生,是因为生成了HBr气体,继续滴加至液溴滴完.装置d的作用是吸收HBr和Br2;
其中发生反应的离子方程式是H++OH-=H2O等(写出一个即可).
(2)上述装置图中,c的名称是冷凝管.
(3)液溴滴完后,经过下列步骤分离提纯:
①向a中加入10mL水,然后过滤除去未反应的铁屑;
②滤液依次用10mL水、8mL10%的NaOH溶液、10mL水洗涤.NaOH溶液洗涤的作用是除去HBr和未反应的Br2;
③向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤.加入氯化钙的目的是干燥.
(4)经以上分离操作后,粗溴苯中还含有的主要杂质为苯,要进一步提纯,还要进行的操作是C(填字母序号).
A.重结晶 B.过滤 C.蒸馏 D.萃取
(5)该实验中,a的容积最适合的是B(填字母序号).
A.25mL B.50mL C.250mL D.500mL.
(6)在该实验中最终制得的纯净溴苯质量为15.7g,则该实验中溴苯的产率为73.85%%(精确到小数点后一位).
14.下列仪器常用于物质分离的是( )


| A. | ③⑤⑥ | B. | ②④⑤ | C. | ②③⑤ | D. | ①②⑥ |
 有机物A常用作有机合成的中间体.15.2g该有机物燃烧生成26.4gCO2和14.4gH2O;质谱图表明其相对分子质量为76,红外光谱分析表明A分子中含有O-H键和C-O键.核磁共振氢谱上有三个峰,峰面积之比为2:1:1.A能发生如图转化:
有机物A常用作有机合成的中间体.15.2g该有机物燃烧生成26.4gCO2和14.4gH2O;质谱图表明其相对分子质量为76,红外光谱分析表明A分子中含有O-H键和C-O键.核磁共振氢谱上有三个峰,峰面积之比为2:1:1.A能发生如图转化: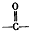 ,则H的结构简式可能为CH3CH2CHO、
,则H的结构简式可能为CH3CH2CHO、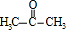 .
.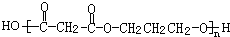 +(2n-1)H2O.
+(2n-1)H2O.